Foram encontradas 36.167 questões.
Uma solução de hidróxido de sódio, a soda cáustica, foi preparada adicionando-se 10,0 mL de uma solução de soda cáustica 15,0 g/L em um balão volumétrico de 250 mL, completando-se o volume adequadamente com água destilada até o traço de aferição. A concentração da solução preparada é igual a
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
A titulação de uma amostra de 25,0 mL de ácido acético impuro (CH3 CO2 H) precisou de 28,0 mL de uma solução de NaOH 0,9 M para chegar ao ponto de equivalência. Com base nessas informações, é correto afirmar que a concentração molar do ácido acético utilizado e sua massa, em gramas, são respectivamente
-
Dados:
• Massa molar do ácido acético: 60,05 g/ mol.
• Massa molar do hidróxido de sódio: 40,00 g/ mol.
Provas
Um técnico preparou duas soluções com quantidades diferentes de soluto e de solvente, e, em seguida, misturou as duas soluções conforme ilustrado a seguir.
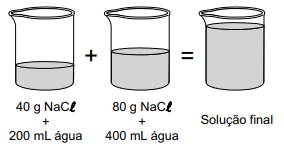
Considerando a operação feita pelo técnico, a solução final obtida tem uma concentração, em g/mL, igual a
Provas
- FundamentosTransformações: Estados Físicos e Fenômenos
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Diferentes líquidos possuem diferentes temperaturas de ebulição. O valor da temperatura de ebulição dos líquidos é influenciado pela pressão atmosférica, cujo valor ao nível do mar é de 1 atm ou 760 mm de Hg. No gráfico a seguir, estão indicadas as temperaturas de ebulição, ao nível do mar, de duas substâncias.
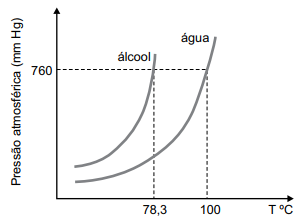
(https://www.policiamilitar.mg.gov.br/conteudoportal/uploadFCK/ctpmbarbacena/31032020102403493.pdf. Adaptado)
Sabendo-se que a pressão atmosférica diminui com a altitude e considerando os dados do gráfico, a água e o álcool, a 1000 m acima do nível do mar,
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Os cálculos envolvendo a concentração de soluções são muito utilizados em práticas médicas, nas atividades periciais, nas indústrias, na produção de medicamentos etc. Esses cálculos determinam a quantidade de soluto que pode ser dissolvida em uma certa quantidade de solvente a uma certa temperatura. No gráfico a seguir, o ponto P indica a quantidade de um soluto (X) que se dissolve em 100 mL de um solvente à temperatura ambiente.
-
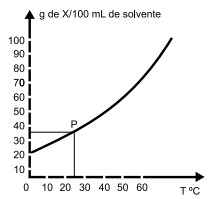
-
(https://www.manualdaquimica.com/ fisico-quimica/calculos-envolvendo-solubilidade.htm#. Adaptado)
-
Se o soluto X é sólido à temperatura ambiente, os pontos de fusão (PF) e ebulição (PE) em ºC dessa substância são:
Provas
Um técnico verificou no laboratório um frasco fechado que continha a seguinte informação:
-
Solução aquosa de NaCl
Volume 1000 mL
-
Como precisava determinar a concentração dessa solução, ele colocou 200 mL dela em um frasco Erlenmeyer e aqueceu até que toda água da solução se evaporou. Utilizou uma balança e mediu a massa total que foi de 451,8 g.
-
Sabendo-se que a massa do Erlenmeyer era de 450,0 g, a concentração da solução do frasco, em g/L, é:
Provas
Solos ácidos apresentam baixo valor de pH, e o plantio de culturas nesse meio acarreta baixa produção agrícola. Entretanto, esse problema pode ser contornado adicionando-se substâncias que, ao entrarem em contato com a água, liberam íons OH−, que neutralizam os íons H3O+ presentes no solo e elevam o seu pH. Para esse objetivo, um agricultor tem comercialmente à disposição as espécies químicas enumeradas:
I – KCl
II – MgO
III – NH4Br
IV – AlCl3
V – P2O5
Para a correção do pH desse solo, o agricultor deverá utilizar a espécie química indicada pelo número
Provas
Diferentemente da respiração aeróbica, alguns microrganismos realizam processos catabólicos que levam à obtenção de moléculas orgânicas de interesse comercial, conforme ilustrado. O conhecimento dessas vias metabólicas é importante, por exemplo, para a fabricação de produtos alimentícios.

Esses processos de fermentação têm em comum a
Provas
Bebidas alcoólicas, algumas soluções desinfetantes ou até álcool combustível são exemplos de misturas constituídas por etanol (CH3CH2OH) e água. A “afinidade” entre esses líquidos é suficiente para possibilitar que a mistura formada por 500 mL de água e 500 mL de etanol origine uma solução de 970 mL, em um processo que envolve liberação de pequena quantidade de energia. De certa forma, isso constitui um problema para os fabricantes, uma vez que, para obterem um litro dessa mistura, necessitariam misturar mais do que 500 mL de cada um dos líquidos.
Do ponto de vista da química, a que se deve essa variação de volume?
Provas
A fim de reaproveitar o resíduo de um processo industrial, cuja composição está indicada, foi proposto um tratamento seguindo o esquema de separações apresentado.
Resíduo dissolvido em éter etílico

ENGEL, R. G. et al. Química orgânica experimental. São Paulo: Cengage Learning, 2012.
Os componentes do resíduo que estão presentes nas frações aquosas II e III são, respectivamente,
Provas
Caderno Container