Foram encontradas 36.278 questões.
Os compostos, mostrados abaixo, pertencem a classe dos álcoois:
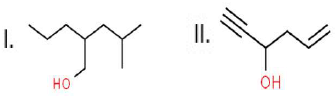
As nomenclaturas para os compostos I e II, respectivamente, segundo a IUPAC, são:
Provas
O produto obtido pela oxidação de um álcool depende da estrutura do álcool. A oxidação de um álcool primário ocorre em duas etapas. Ele é inicialmente oxidado a um composto X, e então, numa segunda etapa, a um composto Y, como mostrado na equação abaixo:
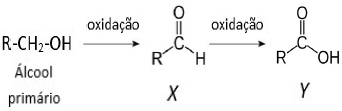
Os produtos X e Y obtidos pela oxidação do álcool acima, respectivamente, são
Provas
Geralmente, os compostos carbonilados são classificados em subcategorias. Esta classificação é feita com base nos grupos ligados ao carbono da carbonila. São exemplos de compostos carbonilados.

Os compostos I, II e III acima apresentam, respectivamente, os grupos funcionais:
Provas
Para descrever as ligações no metano e em outras moléculas, Linus Pauling propôs a teoria da hibridização dos orbitais. Ele propôs que orbitais atômicos s, p e/ou d de um determinado átomo pudessem se misturar para criar um novo conjunto de orbitais, denominado orbitais híbridos. No caso do metano, CH4, cada ligação C-H é formada então pela superposição de um orbital híbrido do carbono com um orbital 1s do hidrogênio. Cada um dos orbitais híbridos do carbono é denominado:
(Dados: 1H1; 6C12)
Provas
Baseado nos conhecimentos adquiridos sobre repulsão de pares de elétrons na camada de valência, RPECV, podemos garantir que o NH3, possui geometria de pares de elétrons e geometria molecular, respectivamente:
(Dados: 1H1; 7N14)
Provas
O modelo de repulsão de pares de elétrons na camada de valência (sigla RPECV, sigla inglesa VSEPR), imaginado por Ronald J. Gillespie (1924-) e Ronald S. Nyholm (1917-1971), é um método confiável de se preverem as formas de moléculas covalentes e de íons poliatômicos. De acordo com esses autores, podemos afirmar CORRETAMENTE que os compostos PF5 e SF4 possuem, respectivamente, geometria molecular:
(Dados: 9F19; 16S32)
Provas
Quando uma reação química ocorre entre dois átomos, os seus elétrons de valência são rearranjados de tal forma que uma força resultante atrativa, a ligação química, passa a existir entre esses átomos. São características de ligação iônica e covalente, respectivamente:
Provas
Sinta-se um químico responsável por um laboratório de Química que deseja preparar 500 mL de uma solução de hidróxido de sódio, NaOH, de concentração 3 mol/L. Qual a quantidade de massa de NaOH que deverá ser pesada e seguidamente dissolvida em água suficiente para completar 500 mL dessa solução?
(Dados: H = 1,00g/mol; Na = 23,00g/mol; O = 16,00g/mol)
Provas
O conceito de concentração é útil em muitos contextos. Por exemplo, o Rio de Janeiro tem cerca de 12 milhões e 800 mil habitantes e área superficial de 46.600 km2, aproximadamente; logo, a concentração média de habitantes é de cerca de 275 habitantes por quilômetro quadrado. Em química, a quantidade de soluto dissolvido num determinado volume de solução pode ser calculada da mesma forma e se denomina concentração da solução. Com base nessas informações, qual a concentração molar da solução preparada de NaCl, quando se usa 116g dessa substância dissolvida em 1000 mL de solução?
(Dados: Na = 23,00g/mol; Cl = 35,00g/mol)
Provas
Os termos “oxidação” e “redução” vêm de reações que foram conhecidas por séculos. Civilizações antigas aprenderam como transformar óxidos e sulfetos metálicos em metais, isto é, como reduzir os minérios em metais. Um exemplo de reações de oxidação-redução, é o óxido de ferro (III) reagindo com o monóxido de carbono, como mostrado na equação abaixo:
Fe2O3 (s) + 3 CO (g) → 2 Fe (s) + 3 CO2 (g)
Nesta reação, podemos afirmar CORRETAMENTE que:
Provas
Caderno Container