Foram encontradas 36.242 questões.
O alaranjado de metila é um corante azoico também conhecido como amarelo-manteiga. É utilizado como indicador em
titulações ácido-base, apresentando coloração vermelha em pH menor que 3,1 e amarela em pH maior que 4,4.
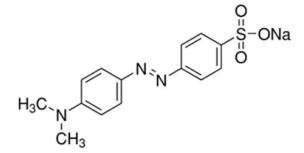
O número de átomos de H em 0,203 mol de alaranjado de metila é:

O número de átomos de H em 0,203 mol de alaranjado de metila é:
Provas
Questão presente nas seguintes provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química Cinética
- Transformações Químicas e EnergiaRadioatividade
As reações nucleares são muito empregadas tanto para gerar eletricidade quanto para criar armas de destruição em massa.
Elas são usadas também para ajudar a determinar os mecanismos de reações químicas, para investigar o movimento de
átomos em sistemas biológicos e para achar a idade de importantes artefatos históricos. A química nuclear é fundamental
para o desenvolvimento da energia nuclear. A química proporciona as técnicas de preparação e recirculação dos combustíveis
nucleares, e de remoção de resíduos radioativos perigosos. Sobre a química nuclear, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Quando o núcleo de urânio-238 perde uma partícula alfa, o fragmento restante tem número atômico 90 e número de massa 234.
( ) Para transformar urânio-238 em rádio-226 foram emitidas 3 partículas beta (β).
( ) A radiação gama consiste em fótons de alta energia; muda a massa e o número atômico de um núcleo.
( ) Quando o rádio-226 sofre decaimento alfa o produto formado é 86Rn222.
A sequência está correta em
( ) Quando o núcleo de urânio-238 perde uma partícula alfa, o fragmento restante tem número atômico 90 e número de massa 234.
( ) Para transformar urânio-238 em rádio-226 foram emitidas 3 partículas beta (β).
( ) A radiação gama consiste em fótons de alta energia; muda a massa e o número atômico de um núcleo.
( ) Quando o rádio-226 sofre decaimento alfa o produto formado é 86Rn222.
A sequência está correta em
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Um professor de química, ao chegar em sua sala de aula, introduziu o conteúdo com a seguinte pergunta: por que o gelo
flutua? E prosseguiu: como ocorre na maioria das substâncias, a fase sólida da parafina é mais densa que a líquida e, por isso,
o sólido afunda sob a superfície do líquido. Em contraste, a fase sólida da água, o gelo, é menos densa que a sua fase líquida,
fazendo com que o gelo flutue na água. A explicação está relacionada aos conceitos de interações intermoleculares e ao
arranjo das moléculas. Então, por que a densidade do gelo é menor do que a densidade da água? Sobre a explicação do
questionamento do professor, analise as afirmativas a seguir.
I. Quando a água congela, as moléculas assumem o arranjo hexagonal aberto e ordenado. Esse arranjo otimiza as interações de ligação de hidrogênio entre as moléculas e cria uma estrutura menos densa para o gelo se comparada com a da água.
II. A densidade mais baixa do gelo comparada com a da água pode ser entendida em termos das interações de ligação de hidrogênio entre as moléculas de água.
III. Uma determinada massa de gelo ocupa maior volume que a mesma massa de água líquida.
Está correto o que se afirma em
I. Quando a água congela, as moléculas assumem o arranjo hexagonal aberto e ordenado. Esse arranjo otimiza as interações de ligação de hidrogênio entre as moléculas e cria uma estrutura menos densa para o gelo se comparada com a da água.
II. A densidade mais baixa do gelo comparada com a da água pode ser entendida em termos das interações de ligação de hidrogênio entre as moléculas de água.
III. Uma determinada massa de gelo ocupa maior volume que a mesma massa de água líquida.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
O professor de química introduziu em sua aula: as sensações de olfato e visão dependem em parte da forma molecular.
Quando você inspira, as moléculas no ar são transportadas pelos sítios receptores em seu nariz. Se as moléculas têm forma e
tamanhos corretos, elas podem se encaixar devidamente nesses sítios receptores, que transmitem impulsos para o cérebro.
O cérebro os identifica como um aroma em particular, como o aroma de pão fresco. O olfato é tão bom em reconhecimento
molecular que duas substâncias podem produzir diferentes sensações de odor mesmo quando suas moléculas diferem tão
sutilmente quanto a mão direita difere da esquerda. Na verdade, o professor quis apresentar um exemplo prático sobre
formas moleculares tridimensionais e o comportamento das moléculas. Após a introdução desse exemplo prático, seguiu
explicando sobre geometria molecular. Posteriormente à explicação, pediu aos alunos que resolvessem a questão elaborada
por ele. Qual será o arranjo, a geometria molecular e a hibridização dos orbitais empregados pelo átomo central para os
compostos hexafluoreto de enxofre e o trifluoreto de cloro, nessa ordem?
Provas
Questão presente nas seguintes provas
Os derivados do petróleo (combustíveis não renováveis) são amplamente utilizados como combustível. Contudo, não são os
únicos combustíveis disponíveis no mercado. Além dos derivados fósseis, podemos encontrar, nos postos de combustível,
etanol, óleo diesel, GNV e, mais recentemente, biodiesel. A combustão completa ou queima de todos os combustíveis fósseis
gera gases poluentes, como o dióxido de carbono, que é considerado por muitos como o principal causador do aquecimento
global:
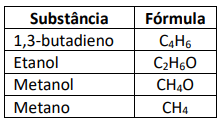
Considerando a combustão completa de 26 g de cada uma das substâncias que podem ser usadas como combustíveis, a substância que irá emitir mais dióxido de carbono é:

Considerando a combustão completa de 26 g de cada uma das substâncias que podem ser usadas como combustíveis, a substância que irá emitir mais dióxido de carbono é:
Provas
Questão presente nas seguintes provas
Um professor de química, após explicar as funções orgânicas, aplicou um desafio para seus alunos. Ele dividiu a turma em
quatro grupos, desenhou uma única estrutura no quadro e, a partir dessa estrutura, entregou um desafio para cada grupo:
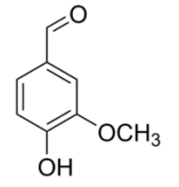
Desafios para os grupos:
1.Quais as funções orgânicas presentes na estrutura desenhada no quadro?
2. Substituindo o –CHO e o –OCH3 por –CH3 e –CH3, qual o nome do composto formado?
3. Substituindo o –CHO e o –OCH3 por –H e COOH, nessa ordem, qual o nome do composto formado?
4. Substituindo o –CHO e o –OH por –H e –H, qual o nome do composto formado?
Sobre as conclusões dos estudantes, marque V para as afirmativas verdadeiras e F para as falsas.
( ) As funções orgânicas presentes na estrutura é álcool, éter e aldeído.
( ) Substituindo –CHO e –OCH3 por –CH3 e –CH3, o nome do composto formado é 2,4-dimetilfenol.
( ) Substituindo –CHO e –OCH3 por –H e COOH, nessa ordem, o nome do composto formado é o hidroxi-benzaldeído.
( ) Substituindo –CHO e –OH por –H e –H, o nome do composto formado é fenil metil éter.
A sequência está correta em

Desafios para os grupos:
1.Quais as funções orgânicas presentes na estrutura desenhada no quadro?
2. Substituindo o –CHO e o –OCH3 por –CH3 e –CH3, qual o nome do composto formado?
3. Substituindo o –CHO e o –OCH3 por –H e COOH, nessa ordem, qual o nome do composto formado?
4. Substituindo o –CHO e o –OH por –H e –H, qual o nome do composto formado?
Sobre as conclusões dos estudantes, marque V para as afirmativas verdadeiras e F para as falsas.
( ) As funções orgânicas presentes na estrutura é álcool, éter e aldeído.
( ) Substituindo –CHO e –OCH3 por –CH3 e –CH3, o nome do composto formado é 2,4-dimetilfenol.
( ) Substituindo –CHO e –OCH3 por –H e COOH, nessa ordem, o nome do composto formado é o hidroxi-benzaldeído.
( ) Substituindo –CHO e –OH por –H e –H, o nome do composto formado é fenil metil éter.
A sequência está correta em
Provas
Questão presente nas seguintes provas
A reação de Baeyer-Villiger, uma reação de oxidação orgânica clássica para converter cetonas a lactonas, é usada na fabricação de plásticos e medicamentos:
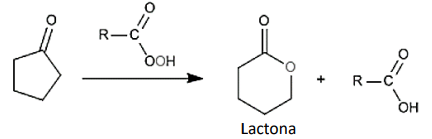
Supondo que a reação ocorra com um rendimento de 78%, qual o número de moléculas da lactona são produzidas, quando se faz reagirem 42 g da cetona? (Considere a estequiometria da reação 1:1.)

Supondo que a reação ocorra com um rendimento de 78%, qual o número de moléculas da lactona são produzidas, quando se faz reagirem 42 g da cetona? (Considere a estequiometria da reação 1:1.)
Provas
Questão presente nas seguintes provas
Após uma aula sobre produção e desenvolvimento de novos materiais e a relação das propriedades desses materiais com a
sua estrutura química, o professor aplicou uma atividade para os estudantes. Ele dividiu a turma em quatro grupos e para
cada grupo entregou a descrição de um material, sua produção, estrutura química e aplicação no mercado, além de uma
pergunta sobre a relação da propriedade do material e da estrutura química desse material. Sugeriu, também, que cada
grupo ao terminar fosse à lousa para descrever a resposta da atividade aplicada. Mais que depressa, o primeiro grupo,
empolgado com a atividade, analisou a pergunta e rapidamente entregou ao professor a resposta. O professor pediu então
a esse grupo que descrevesse o resultado.
Atividade Grupo 1
A produção do Kevlar é feita por meio de um ácido carboxílico (p-benzenodioico) e de uma amina (benzenodiamina). O polímero Kevlar, em virtude de sua alta resistência, que chega a ser, por unidade de massa, cinco vezes maior que a do aço, é utilizado na confecção de coletes à prova de bala. Além disso, a fibra desse polímero é flexível, bastante leve e resistente ao fogo, o que resulta em muitas aplicações, como na confecção de luvas, roupas para bombeiros, equipamentos de proteção para esportes diversos.
Pergunta para o grupo 1: Qual o motivo de tão alta resistência do polímero Kevlar?
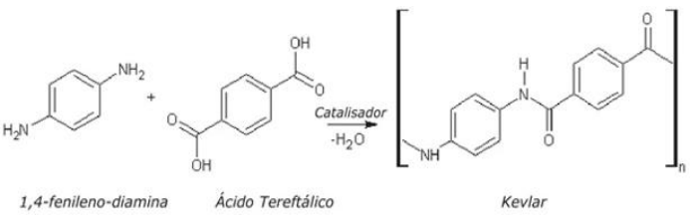
Sobre a resposta da atividade dos alunos do grupo 1, analise as afirmativas a seguir.
I. A substância iônica de alta massa molar confere resistência ao polímero.
II. A alta resistência do polímero está associada à sua capacidade de formar ligações de hidrogênio entre suas moléculas.
III.A alta resistência do polímero está associada à sua capacidade de formar ligações de dispersão de London.
Está correto o que se afirma em
Atividade Grupo 1
A produção do Kevlar é feita por meio de um ácido carboxílico (p-benzenodioico) e de uma amina (benzenodiamina). O polímero Kevlar, em virtude de sua alta resistência, que chega a ser, por unidade de massa, cinco vezes maior que a do aço, é utilizado na confecção de coletes à prova de bala. Além disso, a fibra desse polímero é flexível, bastante leve e resistente ao fogo, o que resulta em muitas aplicações, como na confecção de luvas, roupas para bombeiros, equipamentos de proteção para esportes diversos.
Pergunta para o grupo 1: Qual o motivo de tão alta resistência do polímero Kevlar?

Sobre a resposta da atividade dos alunos do grupo 1, analise as afirmativas a seguir.
I. A substância iônica de alta massa molar confere resistência ao polímero.
II. A alta resistência do polímero está associada à sua capacidade de formar ligações de hidrogênio entre suas moléculas.
III.A alta resistência do polímero está associada à sua capacidade de formar ligações de dispersão de London.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- Química InorgânicaSoluções e Substâncias Inorgânicas
Em seu dia de trabalho, o técnico de laboratório recebeu uma tarefa – realizar quatro experimentos, ou seja, realizar quatro
reações químicas e anotar todas as observações diante de cada reação:
1. Reação de uma solução de ácido clorídrico com raspas de alumínio.
2. Reação entre uma solução de ácido sulfúrico com uma solução de hidróxido de cálcio.
3. Reação entre as soluções de nitrato de chumbo II e iodeto de potássio.
4. Reação entre o carbonato de cálcio e uma solução de ácido clorídrico.
Sobre as observações anotadas pelo técnico de laboratório, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Na reação entre uma solução de ácido clorídrico com raspas de alumínio ocorreu desprendimento de gás.
( ) Na reação entre as soluções de nitrato de chumbo II e iodeto de potássio ocorreu a formação de um precipitado.
( ) Na reação entre uma solução de ácido sulfúrico com uma solução de hidróxido de cálcio formou-se um sal insolúvel.
( ) Na reação entre o carbonato de cálcio e uma solução de ácido clorídrico formou-se o ácido carbônico, um composto estável.
A sequência está correta em
1. Reação de uma solução de ácido clorídrico com raspas de alumínio.
2. Reação entre uma solução de ácido sulfúrico com uma solução de hidróxido de cálcio.
3. Reação entre as soluções de nitrato de chumbo II e iodeto de potássio.
4. Reação entre o carbonato de cálcio e uma solução de ácido clorídrico.
Sobre as observações anotadas pelo técnico de laboratório, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Na reação entre uma solução de ácido clorídrico com raspas de alumínio ocorreu desprendimento de gás.
( ) Na reação entre as soluções de nitrato de chumbo II e iodeto de potássio ocorreu a formação de um precipitado.
( ) Na reação entre uma solução de ácido sulfúrico com uma solução de hidróxido de cálcio formou-se um sal insolúvel.
( ) Na reação entre o carbonato de cálcio e uma solução de ácido clorídrico formou-se o ácido carbônico, um composto estável.
A sequência está correta em
Provas
Questão presente nas seguintes provas
As mudanças químicas podem resultar na liberação ou absorção de calor. Elas também podem provocar a realização de
trabalho, tanto no próprio sistema quanto no sistema da vizinhança. A função termodinâmica chamada entalpia responde
pelo fluxo de calor nas mudanças químicas que ocorrem à pressão constante quando nenhuma forma de trabalho é realizada,
a não ser trabalho PV. Sobre a entalpia, analise as afirmativas a seguir.
I. É uma propriedade extensiva. Portanto, a magnitude do ∆H é diretamente proporcional à quantidade de reagente consumida no processo.
II. A variação de entalpia para uma reação depende do estado dos reagentes e dos produtos.
III.A variação de entalpia para uma reação é igual em valores absolutos, mas oposta em sinais para o ∆H da reação inversa.
Está correto o que se afirma em
I. É uma propriedade extensiva. Portanto, a magnitude do ∆H é diretamente proporcional à quantidade de reagente consumida no processo.
II. A variação de entalpia para uma reação depende do estado dos reagentes e dos produtos.
III.A variação de entalpia para uma reação é igual em valores absolutos, mas oposta em sinais para o ∆H da reação inversa.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container