Foram encontradas 1.181 questões.
Considere a reação química entre os gases SO2(g) e O2(g), responsável por produzir o gás SO3(g), a 1000K. Se as pressões parciais no equilíbrio químico são de SO3= 0,20 bar, SO2= 1,40 bar, e O2=0,80 bar, o valor aproximado da constante de equilíbrio (K) nessa temperatura será de
Provas
- Química CinéticaReações e Soluções
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Suponha que uma solução tenha sido preparada pela mistura dos líquidos A e B. A pressão de vapor do líquido A puro é de 0,26 bar e a pressão de vapor do líquido B puro é de 0,093 bar, ambos à mesma temperatura. A fração molar do líquido B na solução é de 0,60 e o sistema possui espaço vazio. A pressão total do vapor em equilíbrio com a mistura líquida será de
Provas
Considere a reação química hipotética, devidamente balanceada.
3XY(aq) → X3(aq) + 3Y(aq)
Os dados empíricos para a reação supracitada foram monitorados e encontram-se resumidos na Tabela.
|
[XY] mol.L-1 |
Velocidade mol.L-1.s-1 |
|
0,2 |
0,4 |
|
0,4 |
0,4 |
|
0,6 |
0,4 |
A partir das informações fornecidas, a lei de velocidade para a referida reação será de
Provas
- Teorias AtômicasModelos Atômicos. Estrutura do Átomo.
- Teorias AtômicasTabela Periódica. Propriedades periódicas.
Conhecer a configuração eletrônica de um átomo é fundamental, uma vez que ela determina as propriedades químicas dos elementos. Acerca do tema, assinale a alternativa correta.
Provas
Considere um composto básico hipotético, forte, solúvel, nomeado Xa(OH)3, massa molar 55 g/mol. O preparo da solução Xa(OH)3 com concentração 0,01 mol/L resultará no pH aproximado de:
Dados: log 2=0,30, log 3= 0,48, log 5= 0,70
Provas
- Teorias AtômicasModelos Atômicos. Estrutura do Átomo.
- Teorias AtômicasTabela Periódica. Propriedades periódicas.
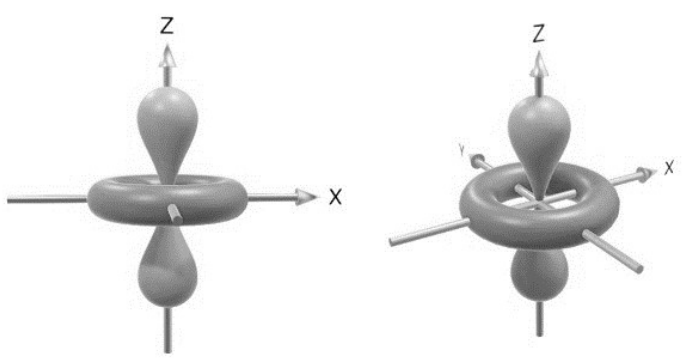
Assinale a alternativa que nomeia corretamente o orbital atômico apresentado nas imagens a seguir.
Provas
Acerca do cálculo da constante de equilíbrio (K) a partir de dados eletroquímicos, analise as assertivas e assinale a alternativa correta.
I. O valor de K pode ser obtido pela expressão matemática ln K = nFEcélula°/RT.
II. Quando K > 1 o valor de Ecélula° deverá ser menor que zero, caracterizando uma reação produto favorecida.
III. Para obter o valor de Ecélula° deve-se determinar Eredução°(Ânodo) - Eredução°(Cátodo).
Provas
A organização dos elementos na tabela periódica é uma das mais notáveis realizações da química, pois permite a sistematização de propriedades que, de outra forma, estariam dispersas em um arranjo caótico. Sobre o desenvolvimento da tabela periódica, assinale a alternativa correta.
Provas
Considere a seguinte equação química não balanceada:
Fe2O3(s) + CO(g) → Fe(s) + CO2(g)
Se 26g de óxido férrico reagir com monóxido de carbono, a massa de ferro produzida será aproximadamente de:
Dados: Fe= 56 g/mol e Fe2O3 = 160 g/mol.
Provas
A respeito da construção do modelo atômico pela mecânica quântica, assinale a alternativa correta.
Provas
Caderno Container