Foram encontradas 200 questões.
A Termodinâmica é a ciência que trata do calor e do trabalho e das propriedades das substâncias relacionadas ao calor e ao trabalho. É objetivo dessa ciência determinar as relações gerais entre a energia interna e outras propriedades internas de um sistema com os parâmetros termodinâmicos (parâmetros macroscópicos que dependem do estado interno de um sistema), associando-as às mudanças no estado do sistema e às suas interações com o ambiente. Julgue o item abaixo, relativos a conceitos e definições da Termodinâmica.
Um processo que ocorre dentro de um sistema envolvido por uma fronteira impermeável ao calor é um processo adiabático, nele não podendo ocorrer fluxo de calor.
Provas
A Termodinâmica é a ciência que trata do calor e do trabalho e das propriedades das substâncias relacionadas ao calor e ao trabalho. É objetivo dessa ciência determinar as relações gerais entre a energia interna e outras propriedades internas de um sistema com os parâmetros termodinâmicos (parâmetros macroscópicos que dependem do estado interno de um sistema), associando-as às mudanças no estado do sistema e às suas interações com o ambiente. Julgue o item abaixo, relativos a conceitos e definições da Termodinâmica.
Um processo realizado de tal modo que ao seu final o sistema e sua vizinhança local sejam restaurados aos seus estados iniciais, sem produzir qualquer mudança no resto do universo, é dito irreversível.
Provas
A Termodinâmica é a ciência que trata do calor e do trabalho e das propriedades das substâncias relacionadas ao calor e ao trabalho. É objetivo dessa ciência determinar as relações gerais entre a energia interna e outras propriedades internas de um sistema com os parâmetros termodinâmicos (parâmetros macroscópicos que dependem do estado interno de um sistema), associando-as às mudanças no estado do sistema e às suas interações com o ambiente. Julgue o item abaixo, relativos a conceitos e definições da Termodinâmica.
Um sistema termodinâmico é uma quantidade de matéria de massa e de características definidas, sobre a qual é dirigida a atenção, separada da vizinhança (tudo o que é externo ao sistema) por meio de fronteiras que podem ser fixas ou móveis.
Provas
O tipo mais comum de corrosão envolve um processo de oxidação eletroquímica de um metal. A perda de elétrons dá origem, dependendo das condições em torno do metal, a outras reações químicas, como, por exemplo, a formação de ferrugem nos aços-carbono. A energia necessária para remover elétrons dos átomos varia de metal para metal, gerando diferentes potenciais de oxidação. Além disso, os elétrons podem ser mais facilmente removidos em certas circunstâncias que em outras. Por exemplo, a presença de água e oxigênio facilita a remoção de elétrons do ferro, assim como os íons cloreto facilitam a retirada de elétrons do alumínio. Ao se fazer contato elétrico entre dois metais (dois eletrodos), um deles, o de maior potencial de eletrodo (catodo), fornecerá elétrons para o circuito, e o outro, o de menor potencial de eletrodo (anodo), receberá os elétrons, formando um circuito elétrico denominado célula galvânica. Para haver corrosão galvânica, é necessário que se forme uma célula galvânica, ou seja, um circuito elétrico formado por um eletrólito e dois elétrodos com potenciais diferentes. A respeito do processo de corrosão eletroquímica, julgue o item a seguir.
A acumulação de sujeiras em superfícies dificulta o acesso de oxigênio, formando um anodo, e contribui para acelerar a corrosão.
Provas
O tipo mais comum de corrosão envolve um processo de oxidação eletroquímica de um metal. A perda de elétrons dá origem, dependendo das condições em torno do metal, a outras reações químicas, como, por exemplo, a formação de ferrugem nos aços-carbono. A energia necessária para remover elétrons dos átomos varia de metal para metal, gerando diferentes potenciais de oxidação. Além disso, os elétrons podem ser mais facilmente removidos em certas circunstâncias que em outras. Por exemplo, a presença de água e oxigênio facilita a remoção de elétrons do ferro, assim como os íons cloreto facilitam a retirada de elétrons do alumínio. Ao se fazer contato elétrico entre dois metais (dois eletrodos), um deles, o de maior potencial de eletrodo (catodo), fornecerá elétrons para o circuito, e o outro, o de menor potencial de eletrodo (anodo), receberá os elétrons, formando um circuito elétrico denominado célula galvânica. Para haver corrosão galvânica, é necessário que se forme uma célula galvânica, ou seja, um circuito elétrico formado por um eletrólito e dois elétrodos com potenciais diferentes. A respeito do processo de corrosão eletroquímica, julgue o item a seguir.
Pode ocorrer corrosão em mecanismos hidráulicos de aço-carbono apoiados em mancais de latão, pois ele pode formar uma célula galvânica de composição tendo o aço como catodo.
Provas
O tipo mais comum de corrosão envolve um processo de oxidação eletroquímica de um metal. A perda de elétrons dá origem, dependendo das condições em torno do metal, a outras reações químicas, como, por exemplo, a formação de ferrugem nos aços-carbono. A energia necessária para remover elétrons dos átomos varia de metal para metal, gerando diferentes potenciais de oxidação. Além disso, os elétrons podem ser mais facilmente removidos em certas circunstâncias que em outras. Por exemplo, a presença de água e oxigênio facilita a remoção de elétrons do ferro, assim como os íons cloreto facilitam a retirada de elétrons do alumínio. Ao se fazer contato elétrico entre dois metais (dois eletrodos), um deles, o de maior potencial de eletrodo (catodo), fornecerá elétrons para o circuito, e o outro, o de menor potencial de eletrodo (anodo), receberá os elétrons, formando um circuito elétrico denominado célula galvânica. Para haver corrosão galvânica, é necessário que se forme uma célula galvânica, ou seja, um circuito elétrico formado por um eletrólito e dois elétrodos com potenciais diferentes. A respeito do processo de corrosão eletroquímica, julgue o item a seguir.
A presença de tensões em componentes estruturais que estejam operando em ambientes corrosivos não afeta a velocidade da corrosão, pois tensões não têminfluência no mecanismo de funcionamento das células galvânicas.
Provas
O tipo mais comum de corrosão envolve um processo de oxidação eletroquímica de um metal. A perda de elétrons dá origem, dependendo das condições em torno do metal, a outras reações químicas, como, por exemplo, a formação de ferrugem nos aços-carbono. A energia necessária para remover elétrons dos átomos varia de metal para metal, gerando diferentes potenciais de oxidação. Além disso, os elétrons podem ser mais facilmente removidos em certas circunstâncias que em outras. Por exemplo, a presença de água e oxigênio facilita a remoção de elétrons do ferro, assim como os íons cloreto facilitam a retirada de elétrons do alumínio. Ao se fazer contato elétrico entre dois metais (dois eletrodos), um deles, o de maior potencial de eletrodo (catodo), fornecerá elétrons para o circuito, e o outro, o de menor potencial de eletrodo (anodo), receberá os elétrons, formando um circuito elétrico denominado célula galvânica. Para haver corrosão galvânica, é necessário que se forme uma célula galvânica, ou seja, um circuito elétrico formado por um eletrólito e dois elétrodos com potenciais diferentes. A respeito do processo de corrosão eletroquímica, julgue o item a seguir.
O mecanismo de eletrodeposição de um metal sobre outro (cromagem, niquelagem etc.) é o mesmo da corrosão. A peça que vai receber a deposição é usada como catodo e uma fonte externa força os elétrons para o catodo, fazendo que os íons liberados pelo anodo, feito do metal a ser depositado, se depositem no catodo.
Provas
O tipo mais comum de corrosão envolve um processo de oxidação eletroquímica de um metal. A perda de elétrons dá origem, dependendo das condições em torno do metal, a outras reações químicas, como, por exemplo, a formação de ferrugem nos aços-carbono. A energia necessária para remover elétrons dos átomos varia de metal para metal, gerando diferentes potenciais de oxidação. Além disso, os elétrons podem ser mais facilmente removidos em certas circunstâncias que em outras. Por exemplo, a presença de água e oxigênio facilita a remoção de elétrons do ferro, assim como os íons cloreto facilitam a retirada de elétrons do alumínio. Ao se fazer contato elétrico entre dois metais (dois eletrodos), um deles, o de maior potencial de eletrodo (catodo), fornecerá elétrons para o circuito, e o outro, o de menor potencial de eletrodo (anodo), receberá os elétrons, formando um circuito elétrico denominado célula galvânica. Para haver corrosão galvânica, é necessário que se forme uma célula galvânica, ou seja, um circuito elétrico formado por um eletrólito e dois elétrodos com potenciais diferentes. A respeito do processo de corrosão eletroquímica, julgue o item a seguir.
A umidade do ar atmosférico é insuficiente para permitir a formação de uma célula galvânica na superfície de uma peça de aço-carbono e enferrujá-la.
Provas
Texto CI-I – questões 13 e 14
Um empregado de uma empresa está elaborando, com o auxílio do editor de textos Word 97, um glossário contendo termos técnicos. A janela mostrada na figura abaixo apresenta parte do referido documento, ainda na fase de edição.
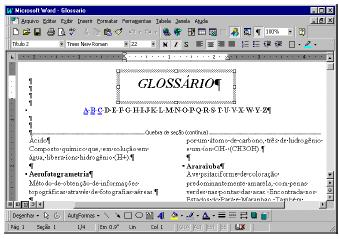
A partir da figura, pode-se concluir que, para a digitação dos termos técnicos na forma mostrada na área de trabalho do Word 97, o empregado inseriu uma tabela com duas colunas e várias linhas.
Provas
Nas questões de 11 a 15, considere que todos os programas mencionados estão em configuração-padrão, em português, e que o mouse está configurado para pessoas destras. Assim, a menos que seja explicitamente informado o contrário, expressões como clicar, clique simples e clique duplo referem-se a cliques com o botão esquerdo do mouse. Considere também que não há restrições de proteção e de uso em relação aos programas, arquivos, diretórios e hardware utilizados.

A figura acima ilustra a área de trabalho (desktop) de um determinado computador cujo sistema operacional é o Windows 98. Entre as ferramentas disponíveis no Windows 98, encontra-se o Active Desktop, que torna possível personalizar o desktop e integrá-lo à Web. Com o Active Desktop, pode-se transformar elementos da Web em elementos da área de trabalho, como pode ser observado na figura acima, na qual duas janelas estão integradas ao desktop, realizando o acesso por meio da Internet a páginas dos sites http://www.petrobras.com.br e http://www.cespe.unb.br. Com base na figura acima, julgue os itens seguintes, acerca do Windows 98 e de suas diversas ferramentas.
Versões atuais do Windows 98 permitem o compartilhamento de uma conexão à Internet com vários computadores em uma rede doméstica.
Provas
Caderno Container