Foram encontradas 100 questões.
H2(g) → 2H+ (aq) + 2e− E0 = 0,00 V
2Ag+ (aq) + 2e− 2Ag0 (s) E0 = +0,80 V
O eletrodo de hidrogênio é constituído por gás hidrogênio borbulhado em solução de ácido clorídrico. Admitindo um eletrodo de hidrogênio formando pilha com um eletrodo de prata e de acordo com as semirreações apresentadas acima, tem-se que o(a)
Provas
2H+ (aq) + 2e− H2(g) E0 = 0,00V
Ag+ (aq) + e− Ag0 (s) E0 = +0,80V
Zn2+ (aq) + 2e− Zn0 (s) E0 = −0,76V
Dadas as semiequações de redução e seus respectivos potenciais eletroquímicos acima, tem-se que
Provas
Considere as afirmações a seguir sobre coloides.
I – Um coloide liófilo, que tem camada de solvatação por sua própria natureza, é sempre mais estável que um coloide liófobo, que não a possui.
II – Amido em água é um exemplo de coloide molecular.
III – Em uma solução coloidal, a passagem de solução para gel é chamada pectização.
IV – Uma solução coloidal é mais estável se as partículas possuirem cargas elétricas com sinais opostos.
V – As partículas coloidais movimentam-se em ziguezague, em decorrência dos choques que sofrem das moléculas do dispersante.
São corretas APENAS as afirmações
Provas
Uma determinada solução apresenta concentração hidroxiliônica igual a 10−10. Esta solução
Provas
Qual das seguintes características corresponde ao fluxo de elétrons da pilha eletroquímica?
Provas
O gráfico a seguir representa a curva de solubilidade de quatro substâncias.
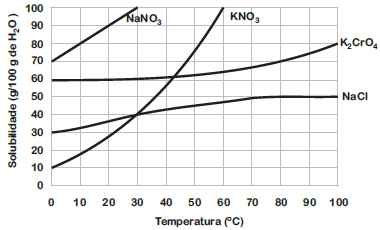
Analisando o gráfico, NÃO se pode concluir que
Provas
O dióxido de carbono, produto da queima completa de combustíveis fósseis, é de grande relevância no fenômeno de aumento da temperatura global. Uma alternativa de mitigação é seu sequestro por submersão nas profundezas dos oceanos e sua reação, em meio aquoso, com carbonato de cálcio sólido para produção de bicarbonato de cálcio solúvel. Considerando a queima completa de 1,0 Kg de carvão 96%, qual a massa, em kg, de bicarbonato de cálcio produzida? (Dados: HMA= 1, CMA= 12, OMA= 16, CaMA= 41)
Provas
As reações químicas podem ser classificadas em função da natureza das substâncias que participam da reação. Atende ao critério de classificação de reações químicas o seguinte conceito ou exemplo de reação:
Provas
Sobre ligações químicas entre átomos, analise as afirmações a seguir.
I – Ligações iônicas ocorrem, geralmente, entre átomos de metais e não metais.
II – Quando a molécula é formada por duas ou mais ligações covalentes polares, ela é apolar, se essas ligações se distribuírem, assimetricamente, no espaço.
III – Ligações covalentes ocorrem, geralmente, entre átomos de não metais.
IV – Quando uma molécula é formada por uma ou mais ligações apolares, igualmente distribuídas no espaço, ela é apolar.
V – Ligação metálica é a ligação que ocorre entre átomos de metais.
São corretas APENAS as afirmações
Provas
Durante a operação de preparo de uma solução ácida em uma refinaria, 4,9 Kg de ácido sulfúrico vazaram, tendo sido imediatamente neutralizados com hidróxido de sódio. Qual é a massa de hidróxido de sódio, em kg, reagida?
(Dados: HMA= 1, SMA= 32, OMA= 16, NaMA= 23)
Provas
Caderno Container