Foram encontradas 100 questões.
A reforma catalítica é um importante processo industrial usado para aumentar o número de octanagem da gasolina e produzir aromáticos por meio de aquecimento e catalisadores apropriados. O benzeno, por exemplo, pode ser obtido a partir do n-hexano por meio da seguinte reação:
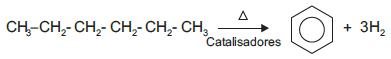
Nesse processo, átomos de hidrogênio são retirados da molécula do n-hexano para a formação do anel benzênico, caracterizando uma reação de eliminação conhecida como
Provas
Os polímeros vinílicos são polímeros de adição, cujos monômeros apresentam o grupamento vinila [CH2 = CH –] em sua composição. Um desses polímeros é o poliestireno, utilizado na fabricação de embalagens, pratos, copos, etc. Dentre as estruturas moleculares relacionadas, a que apresenta o monômero do poliestireno é
Provas
Uma corrente de água residuária, em sua fase final de tratamento, apresentava pH igual a 3,6. Para que pudesse ser disposta no ambiente de forma adequada, essa corrente passou por uma etapa de correção de seu pH, que foi para 6,7. Após a correção do pH, a [H+] na água residuária
Provas
O óxido de cálcio reage com água formando a cal hidratada, de acordo com a seguinte reação:
CaO + H2O → Ca(OH)2 + 63.7 kJ/mol de CaO
Essa característica de reagir com a água formando uma base também é apresentada por
Provas
As reações apresentadas a seguir são provenientes da presença do sulfeto de hidrogênio (H2S) em alguns processos industriais.
I - 2 NaOH + H2S → Na2S + 2 H2O
II - H2S + 3/2 O2 → SO2 + H2O
III - FeCl2 + H2S → 2 HCl + FeS
IV - Fe + H2S → FeS + H2
Apresentam processos de oxirredução,ou seja, transferências de elétrons, APENAS as reações
Provas
Uma solução de salmoura foi preparada em um tanque misturando-se 600 L de HCl 0,2 M com 400 L de NaOH 0,3 M. Desprezando-se o volume de água formado na reação, a concentração, em molaridade (M), da solução final em relação ao sal formado foi
Provas
O gás clorídrico (HCl) é uma substância gasosa formada por moléculas polares. A formação de uma solução aquosa desse gás ocorre pela ionização de suas moléculas, por meio de uma reação com a água, provocando a formação dos íons H3O+ e Cl−. Dentre as substâncias relacionadas, a que passa pelo mesmo processo de dissolução que o HCl para formar uma solução aquosa é
Provas
A expressão da constante de equilíbrio, em termos de concentração de produtos e reagentes, de uma das etapas para a obtenção industrial do ácido sulfúrico é dada por
!$ K_c=dfrac{[SO_3]^2}{[SO_2]^2[O_2]} !$
A equação da reação química representada pela expressão dessa constante de equilíbrio é
Provas
A célula a combustível de hidrogênio funciona pela reação de combustão entre o hidrogênio e o oxigênio, produzindo água. Como eletrólito, emprega-se uma solução aquosa concentrada de KOH. A reação global do processo é representada pela equação H2 + ½ O2 → H2O. Essa equação é obtida por meio das semirreações que ocorrem nos eletrodos da célula. No catodo, a equação da semirreação é ½ O2 + H2 O + 2 e− 2 OH− e, no anodo, a equação é
Provas
A água oxigenada ou peróxido de hidrogênio (H2O2) pode atuar tanto como oxidante quanto como redutor, dependendo do meio em que se encontra, como pode ser visto nas seguintes reações:
H2O2 + H2 SO4 + KMnO4 → K2 SO4 + MnSO4 + H2O + O2 H2O2 + KCl → Cl2 + KOH
Essa característica pode ser atribuída, principalmente, ao fato de o oxigênio, nesse composto, possuir estado de oxidação igual a
Provas
Caderno Container