Foram encontradas 50 questões.
Observe o gráfico a seguir.
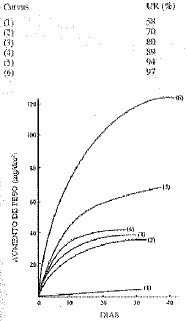
O gráfico acima evidencia a influência de deposição de partículas de NaCl em superfícies de ferro, em diferentes valores de umidade relativa.
Analisando o gráfico, é correto afirmar que
Provas
Analise a tabela a seguir.
| Padrões (mg/L) | Absorbância |
| 0 1 | 0,000 0,200 |
| 2 3 | 0,400 0,600 |
| 4 | 0,800 |
Na tabela acima são apresentadas as concentrações dos padrões analíticos de uma substância hipotética utilizada e seus respectivos valores de absorbância. Qual a concentração dessa substância hipotética para uma amostra que apresentou uma absorbância de 0,425?
Provas
Coloque F (falso) ou V (verdadeiro)nas afirmativas abaixo, em relação à potenciometria, assinalando, a seguir, a opção correta.
I - Potenciometria é uma aplicação analítica direta da equação de Nernst, medindo-se os potenciais de elétrodos polarizados em condições de corrente zero.
II - A equação de Nernst fornece uma relação simples entre o potencial relativo de um elétrodo e a concentração das espécies iônicas correspondentes em solução.
III- O mais importante elétrodo sensível ao pH é o elétrodo de vidro. Esse dispositivo se baseia no fato de membranas delgadas de certas variedades de vidro serem suscetíveis aos íons-hidrogênio.
Provas
Considere os seguintes dados: Kps AgCl = 1,5.10-10 e Kps Ag2CrO4 = 3,2.10-12
Adicionando-se AgNO3 0,1M a uma solução que é 0,1M, em relação ao cloreto, e 2.10-3 M, em relação ao cromato, e correto afirmar que:
Provas
Uma solução aquosa saturada de gás sulfídrico possui concentração igual a 0,1M e constante de ionização igual a 10-22. Calcule a concentração de sulfeto necessária para precipitação dos cátions do segundo Grupo, sabendo-se que o pH deve ser regulado para se obter uma solução 0,25M em ácido clorídrico, e assinale a opção correta.
Dados: H2S → 2 H+ + S-2
Provas
Analise as equações a seguir.
I - HF + H2O → H3O+ + F-
II - HCl + NH3 → NH4+ + Cl-
III- HNO3 + H2O → H3O+ + NO3-
De acordo com o conceito de ácido-base de Bronsted-Lowry, é INCORRETO afirmar que na equação
Provas
Em um becher, contendo solução aquosa 3% de NaCl, juntou-se 1ml de solução aquosa-alcoólica de fenolftaleína e 2ml de solução aquosa 1N de ferricianeto de potássio. Foram emergidos neste becher 3 eletrodos metálicos, sendo um de cobre, um de ferro e outro de zinco, ligados por um fio condutor. Decorridos alguns minutos, observou-se uma coloração róseo-avermelhada em torno dos eletrodos de ferro e cobre, e resíduo esbranquiçado em torno do eletrodo de zinco. De acordo com essas informações, é correto afirmar que o
Provas
De acordo com as suas propriedades ácido-base, os óxidos podem ser classificados em ácidos, básicos, anfóteros ou neutros. Assinale a opção que apresenta, respectivamente, a classificação dos seguintes óxidos: Na2O, N2O5, ZnO, e CO.
Provas
Analise o esquema a seguir.

O esquema simplificado acima mostra as etapas percorridas por uma solução contendo os cátions: Al+3, Ag+1, Ca+2, Cu+2.
As letras A, B, C e D representam, respectivamente, os cátions:
Provas
Coloque F (falso) ou V (verdadeiro) nas afirmativas abaixo, em relação à isomeria, assinalando, a seguir, a opção correta.
( ) Isômeros são compostos diferentes que tem a mesma fórmula molecular.
( ) cis-1,2 dicloroeteno e trans-1,2 dicloroeteno, são exemplos de estereoisômero.
( ) enantiômeros são estereoisômeros cujas moléculas não são imagens especulares uma da outra e que não se superpõem.
( ) Uma molécula quiral é aquela que é idêntica a sua imagem no espelho.
( ) Etanol e éter dimetílico são exemplos de estereoisômero.
Provas
Caderno Container