Foram encontradas 105 questões.
Considere as seguintes configurações eletrônicas de espécies no estado gasoso:
I. !$ 1s^22s^22p^1 !$.
II. !$ 1s^22s^22p^3 !$.
III. !$ 1s^22s^22p^4 !$.
IV. !$ 1s^22s^22p^5 !$.
V. !$ 1s^22s^22p^53s^1 !$.
Assinale a alternativa ERRADA.
Provas
Considere as seguintes afirmações relativas ao gráfico apresentado abaixo:
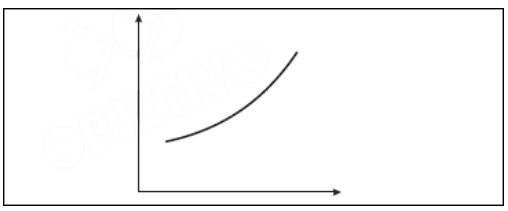
I. Se a ordenada representar a constante de equilíbrio de uma reação química exotérmica e a abscissa, a temperatura, o gráfico pode representar um trecho da curva relativa ao efeito da temperatura sobre a constante de equilíbrio dessa reação.
II. Se a ordenada representar a massa de um catalisador existente em um sistema reagente e a abscissa, o tempo, o gráfico pode representar um trecho relativo à variação da massa do catalisador em função do tempo de uma reação.
III.Se a ordenada representar a concentração de um sal em solução aquosa e a abscissa, a temperatura, o gráfico pode representar um trecho da curva de solubilidade deste sal em água.
IV. Se a ordenada representar a pressão de vapor de um equilíbrio líquido !$ \rightleftarrows !$ gás e a abscissa, a temperatura, o gráfico pode representar um trecho da curva de pressão de vapor deste líquido.
V. Se a ordenada representar a concentração de !$ NO_2 (g) !$ existente dentro de um cilindro provido de um pistão móvel, sem atrito, onde se estabeleceu o equilíbrio !$ N_2O_4(g) !$ !$ \rightleftarrows !$ !$ 2NO_2(g) !$, e a abscissa, a pressão externa exercida sobre o pistão, o gráfico pode representar um trecho da curva relativa à variação da concentração de !$ NO_2 !$ em função da pressão externa exercida sobre o pistão, à temperatura constante.
Destas afirmações, estão CORRETAS
Provas
Seja S a solubilidade de !$ Ag_3PO_4 !$ em 100g de água pura numa dada temperatura. A seguir, para a mesma temperatura, são feitas as seguintes afirmações a respeito da solubilidade de !$ Ag_3PO_4 !$ em 100g de diferentes soluções aquosas:
I. A solubilidade do !$ Ag_3PO_4 !$ em solução aquosa 1 mol/L de !$ HNO_3 !$ é maior do que S.
II. A solubilidade do !$ Ag_3PO_4 !$ em solução aquosa 1 mol/L de !$ AgNO_3 !$ é menor do que S.
III.A solubilidade do !$ Ag_3PO_4 !$ em solução aquosa 1 mol/L de !$ Na_3PO_4 !$ é menor do que S.
IV.A solubilidade do !$ Ag_3PO_4 !$ em solução aquosa 1 mol/L de KCN é maior do que S.
V. A solubilidade do !$ Ag_3PO_4 !$ em solução aquosa 1 mol/L de !$ NaNO_3 !$ é praticamente igual a S.
Destas afirmações, estão CORRETAS
Provas
A equação química que representa a reação de decomposição do iodeto de hidrogênio é:
!$ 2 \,HI (g) \rightarrow H_2 (g) + I_2 (g) !$; !$ Δ H (25°C) = – 51,9 \, kJ !$.
Em relação a esta reação, são fornecidas as seguintes informações:
a) A variação da energia de ativação aparente dessa reação ocorrendo em meio homogêneo é igual a 183,9 kJ.
b) A variação da energia de ativação aparente dessa reação ocorrendo na superfície de um fio de ouro é igual a 96,2 kJ.
Considere, agora, as seguintes afirmações relativas a essa reação de decomposição:
I. A velocidade da reação no meio homogêneo é igual a da mesma reação realizada no meio heterogêneo.
II. A velocidade da reação no meio homogêneo diminui com o aumento da temperatura.
III.A velocidade da reação no meio heterogêneo independe da concentração inicial de iodeto de hidrogênio.
IV. A velocidade da reação na superfície do ouro independe da área superficial do ouro.
V. A constante de velocidade da reação realizada no meio homogêneo é igual a da mesma reação realizada no meio heterogêneo.
Destas afirmações, estão CORRETAS
Provas
Um elemento galvânico é constituído pelos eletrodos abaixo especificados e separados por uma ponte salina.
ELETRODO I: placa de chumbo metálico mergulhada em uma solução aquosa 1 mol/L de nitrato de chumbo.
ELETRODO II: sulfato de chumbo sólido prensado contra uma “peneira” de chumbo metálico mergulhada em uma solução aquosa 1 mol/L de ácido sulfúrico.
Nas condições-padrão, o potencial de cada um destes eletrodos, em relação ao eletrodo padrão de hidrogênio, é
!$ E^°_ {Pb/Pb^{2+}} !$ = – 0,1264 V (ELETRODO I).
!$ E^°_{ Pb/PbSO_4,SO_4 ^{2- }} !$ = – 0,3546 V (ELETRODO II).
Assinale a opção que contém a afirmação CORRETA sobre as alterações ocorridas neste elemento galvânico quando os dois eletrodos são conectados por um fio de baixa resistência elétrica e circular corrente elétrica no elemento.
Provas
Considere as soluções aquosas obtidas pela dissolução das seguintes quantidades de solutos em um 1L de água:
I. 1 mol de acetato de sódio e 1 mol de ácido acético.
II. 2 mols de amônia e 1 mol de ácido clorídrico.
III. 2 mols de ácido acético e 1 mol de hidróxido de sódio.
IV. 1 mol de hidróxido de sódio e 1 mol de ácido clorídrico
V. 1 mol de hidróxido de amônio e 1 mol de ácido acético.
Das soluções obtidas, apresentam efeito tamponante
Provas
A massa de um certo hidrocarboneto é igual a 2,60g. As concentrações, em porcentagem em massa, de carbono e de hidrogênio neste hidrocarboneto são iguais a 82,7% e 17 ,3%, respectivamente. A fórmula molecular do hidrocarboneto é
Provas
O frasco mostrado na figura a seguir contém uma solução aquosa saturada em oxigênio, em contato com ar atmosférico, sob pressão de 1 atm e temperatura de 25°C.
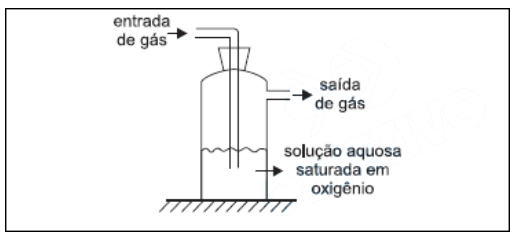
Quando gás é borbulhado através desta solução, sendo a pressão de entrada do gás maior do que a pressão de saída, de tal forma que a pressão do gás em contato com a solução possa ser considerada constante e igual a 1 atm, é ERRADO afirmar que a concentração de oxigênio dissolvido na solução
Provas
Considere uma reação química representada pela equação: Reagentes !$ \rightarrow !$ Produtos. A figura abaixo mostra esquematicamente como varia a energia potencial !$ (E_p) !$ deste sistema reagente em função do avanço da reação química. As letras a, b, c, d e e representam diferenças de energia.
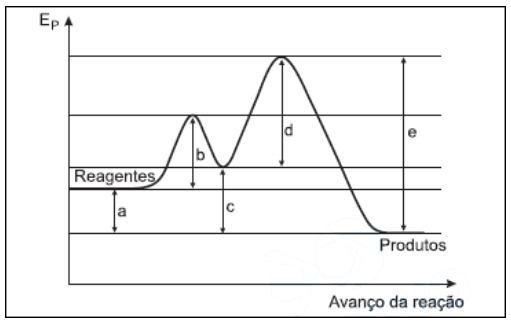
Com base nas informações apresentadas na figura é CORRETO afirmar que
Provas
Assinale a opção que apresenta um par de substâncias isomorfas.
Provas
Caderno Container