Foram encontradas 2.250 questões.
Em ambientes biológicos, a diferença de concentração de solutos entre o interior da célula e o meio externo
está diretamente relacionada à pressão osmótica. Quando uma célula animal é colocada em uma solução
hipertônica, ocorre perda de água para o meio, levando à retração celular. Já em soluções hipotônicas, a
entrada excessiva de água pode provocar o rompimento da membrana plasmática. A variação de volume
celular em meios com diferentes concentrações de solutos ocorre devido ao fato de que a pressão osmótica
Provas
Questão presente nas seguintes provas
O tratamento de água de piscinas com compostos à base de cloro, como o hipoclorito de cálcio (Ca(OCl)₂),
pode elevar o pH do meio devido à hidrólise do íon hipoclorito (OCl⁻). Para neutralizar a alcalinidade, um sal de
caráter ácido, como o hidrogenossulfato de sódio (NaHSO₄), é adicionado.
Em uma piscina com 5,0 × 10⁵ litros de água, foram adicionados 1,2 kg de NaHSO₄. Assumindo a dissociação iônica completa do sal em solução e considerando as massas molares para Na, H, S e O como 23 g/mol, 1 g/mol, 32 g/mol e 16 g/mol, respectivamente, a concentração em mol por litro do íon sódio (Na⁺) resultante é
Em uma piscina com 5,0 × 10⁵ litros de água, foram adicionados 1,2 kg de NaHSO₄. Assumindo a dissociação iônica completa do sal em solução e considerando as massas molares para Na, H, S e O como 23 g/mol, 1 g/mol, 32 g/mol e 16 g/mol, respectivamente, a concentração em mol por litro do íon sódio (Na⁺) resultante é
Provas
Questão presente nas seguintes provas
No modelo de Bohr do átomo de Hidrogênio, o elétron pode ocupar somente determinados níveis de energia.
Tomando como base seu modelo atômico, o valor aproximado do comprimento de onda observado quando um
elétron parte do estado de energia n = 4 para o estado de energia n = 2 é igual a
Dados: Constante de Plank (h): 6,626 x 10 -34 J.s Velocidade da Luz (c): 2,998 x 10 8 m.s -1 Constante de Rydberg (R): 1,0974 x 10 7 m-1
Dados: Constante de Plank (h): 6,626 x 10 -34 J.s Velocidade da Luz (c): 2,998 x 10 8 m.s -1 Constante de Rydberg (R): 1,0974 x 10 7 m-1
Provas
Questão presente nas seguintes provas
Em sua essência, o Princípio da Incerteza de Heisenberg afirma que é impossível conhecer com precisão
absoluta e, simultaneamente, a posição e o momento (quantidade de movimento) de uma partícula subatômica.
Levando-se em consideração este princípio, pode-se calcular que a incerteza mínima na posição de um elétron
com massa de 9,1 x 10
-28g, cuja velocidade é conhecida com uma incerteza de 2,0 x 10
-2 m.s
-1 é
Dados: Constante de Plank (h) = 6,626 x 10 -34 kg.m2 /s Pi (ᴨ) = 3,14
Dados: Constante de Plank (h) = 6,626 x 10 -34 kg.m2 /s Pi (ᴨ) = 3,14
Provas
Questão presente nas seguintes provas
A energia livre de Gibbs representa a máxima energia disponível para a realização de trabalho. A tabela a
seguir mostra os valores termodinâmicos para cálculo do ΔGº
reação
Tabela - Valores Termodinâmicos.

(Fonte: KOTZ, J. C., TREICHEL, P. M., WEAVER, G. C. Química Geral e Reações Químicas, v.1. São Paulo: Cengage Learning, 2010).
Utilizando os valores de ΔH º f e Sº disponibilizados nessa tabela, o ΔGº reação para reação de formação de etino a 298K é de, aproximadamente:
Tabela - Valores Termodinâmicos.

(Fonte: KOTZ, J. C., TREICHEL, P. M., WEAVER, G. C. Química Geral e Reações Químicas, v.1. São Paulo: Cengage Learning, 2010).
Utilizando os valores de ΔH º f e Sº disponibilizados nessa tabela, o ΔGº reação para reação de formação de etino a 298K é de, aproximadamente:
Provas
Questão presente nas seguintes provas
O ciclo do nitrogênio permite a ciclagem deste elemento no ambiente, disponibilizando-o para os seres vivos.
Os animais necessitam do nitrogênio incorporado em compostos orgânicos, enquanto plantas e algas
necessitam do nitrogênio sob a forma de íons nitrato ou amônio. Sobre este ciclo biogeoquímico, é correto
afirmar que a
Provas
Questão presente nas seguintes provas
Em uma certa reação química, obteve-se como um dos produtos uma substância gasosa. Após análise, foi
comprovado que tinha em sua massa 80% de carbono e 20% de hidrogênio. Verificou-se também que 0,5 L do
gás, nas CNTP, pesava 670 mg. A partir desses valores, considerando a constante dos gases ideais como
sendo R = 0,082 L.atm/K.mol, conclui-se que o valor aproximado da massa molar do gás e sua fórmula
empírica e molecular, respectivamente, são
Provas
Questão presente nas seguintes provas
Considere os dados apresentados a seguir.
CH3CH2CHO(g) + H2 (g) -→ CH3CH2CH2OH(g)
Tabela - Dados das Energias de Ligação Médias para ligações Simples e Múltiplas
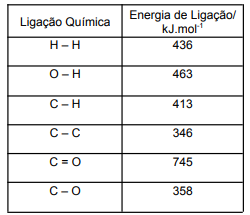
(Fonte: KOTZ, J. C., TREICHEL, P. M., WEAVER, G. C. Química Geral e Reações Químicas, v.1. São Paulo: Cengage Learning, 2010.)
Estima-se que o valor da entalpia para reação de hidrogenação do propanal é:
Provas
Questão presente nas seguintes provas
As reações químicas em um airbag envolvem a decomposição da azida de sódio para gerar o gás nitrogênio, o
qual infla o airbag. A reação principal envolve a azida de sódio, que se decompõe em sódio metálico e
nitrogênio gasoso, conforme a reação (equação 1). À medida que o gás nitrogênio produzido infla o airbag, o
sódio metálico vai sendo neutralizado por outras substâncias, conforme representado pela equação 2 a seguir.
NaN3 (s) → Na(s) + N2 (g) (Equação 1).
Na + KNO3 → K2O + Na2O + N2 (Equação 2).
Após o devido balanceamento das equações, ao se decompor 15 g de NaN3 , e sabendo que todo o sódio metálico formado na equação 1 será consumido na equação 2, a massa de N2 e o seu volume nas Condições Normais de Temperatura e Pressão (CNTP) obtidos, respectivamente, serão
NaN3 (s) → Na(s) + N2 (g) (Equação 1).
Na + KNO3 → K2O + Na2O + N2 (Equação 2).
Após o devido balanceamento das equações, ao se decompor 15 g de NaN3 , e sabendo que todo o sódio metálico formado na equação 1 será consumido na equação 2, a massa de N2 e o seu volume nas Condições Normais de Temperatura e Pressão (CNTP) obtidos, respectivamente, serão
Provas
Questão presente nas seguintes provas
Segundo John C. Kotz em seu livro Química Geral e Reações Químicas, nem todas as reações redox
envolvem o oxigênio, mas todas as reações de oxidação e redução envolvem a transferência de elétrons entre
as substâncias. Estas reações são importantes e têm muitas aplicações no nosso cotidiano, por exemplo, na
obtenção de metais nos processos industriais e em reações nos organismos vivos. Dada a equação a seguir,
SO4
2- (aq) + 2CH2O(aq) + 2H
+
(aq) → H2S(aq) + 2CO2
(g) + 2H2O(l), é correto afirmar que
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container