Foram encontradas 60 questões.
Em estudos clínicos utilizando seres humanos, como os de
biodisponibilidade e bioequivalência, a presença do
pesquisador principal é essencial. É responsabilidade de o
investigador principal garantir os direitos e bem estar dos
sujeitos da pesquisa, obtendo de forma correta, e no
momento adequado, a assinatura do Termo de
Consentimento Livre e Esclarecido. Pode-se dizer que não é
responsabilidade do investigador principal:
Provas
Questão presente nas seguintes provas
Sobre farmacovigilância, analise as afirmativas a seguir.
I. A notificação voluntária é classificada como um processo de vigilância passiva e as instituições sentinela são classificados como vigilância ativa.
II. Conceitos e métodos epidemiológicos são utilizados na farmacovigilância.
III. A notificação de suspeita de reação adversa só deve ser realizada, quando da certeza de que a reação ocorreu devido ao uso de um medicamento.
IV. A avaliação da causalidade só pode ser realizada por meio do uso de algoritmos.
Assinale:
I. A notificação voluntária é classificada como um processo de vigilância passiva e as instituições sentinela são classificados como vigilância ativa.
II. Conceitos e métodos epidemiológicos são utilizados na farmacovigilância.
III. A notificação de suspeita de reação adversa só deve ser realizada, quando da certeza de que a reação ocorreu devido ao uso de um medicamento.
IV. A avaliação da causalidade só pode ser realizada por meio do uso de algoritmos.
Assinale:
Provas
Questão presente nas seguintes provas
Com relação ao estrutura de proteínas, analise afirmativas a seguir.
I. Exceto alguns casos raros, os aminoácidos que são incorporados às proteínas desviam o plano da luz polarizada para a direita.
II. Exceto alguns casos raros, os aminoácidos que são incorporados às proteínas desviam o plano da luz polarizada para a esquerda.
III. Exceto alguns casos raros, os aminoácidos que são incorporados às proteínas não desviam o plano da luz polarizada.
Assinale:
I. Exceto alguns casos raros, os aminoácidos que são incorporados às proteínas desviam o plano da luz polarizada para a direita.
II. Exceto alguns casos raros, os aminoácidos que são incorporados às proteínas desviam o plano da luz polarizada para a esquerda.
III. Exceto alguns casos raros, os aminoácidos que são incorporados às proteínas não desviam o plano da luz polarizada.
Assinale:
Provas
Questão presente nas seguintes provas
Com relação às evidências utilizadas na predição de genes codificantes em genomas procariotos, analise as afirmativas a seguir.
I. Identificação, em outros genomas, de sequências protéicas homólogas as codificada por ORFs (quadros abertos de leitura) presentes no genoma analisado.
II. Identificação de íntrons, trechos ricos em GC e menores que 100 pb, localizados dentro de ORFs presentes no genoma analisado.
III. Comparação do conteúdo de GC e da frequência de códons das ORFs presentes no genoma analisado com a de genes codificantes já descritos para a mesma espécie.
IV. Identificação de junções éxon-íntron nas ORFs presentes no genoma analisado.
Assinale:
I. Identificação, em outros genomas, de sequências protéicas homólogas as codificada por ORFs (quadros abertos de leitura) presentes no genoma analisado.
II. Identificação de íntrons, trechos ricos em GC e menores que 100 pb, localizados dentro de ORFs presentes no genoma analisado.
III. Comparação do conteúdo de GC e da frequência de códons das ORFs presentes no genoma analisado com a de genes codificantes já descritos para a mesma espécie.
IV. Identificação de junções éxon-íntron nas ORFs presentes no genoma analisado.
Assinale:
Provas
Questão presente nas seguintes provas
Sobre biodisponibilidade, analise as afirmativas a seguir.
I. A biodisponibilidade é menor do que 100% para fármacos que não são administrados por via intravenosa.
II. A área sob a curva (ASC) é o parâmetro farmacocinético usado para avaliar a biodisponibilidade absoluta.
III. Medicamentos de uso oral cujos fármacos não sejam absorvidos no trato gastrintestinal não necessitam de estudos de biodisponibilidade relativa.
IV. A biodisponibilidade traduz a velocidade e a extensão de absorção de um fármaco a partir de uma forma de administração.
Assinale:
I. A biodisponibilidade é menor do que 100% para fármacos que não são administrados por via intravenosa.
II. A área sob a curva (ASC) é o parâmetro farmacocinético usado para avaliar a biodisponibilidade absoluta.
III. Medicamentos de uso oral cujos fármacos não sejam absorvidos no trato gastrintestinal não necessitam de estudos de biodisponibilidade relativa.
IV. A biodisponibilidade traduz a velocidade e a extensão de absorção de um fármaco a partir de uma forma de administração.
Assinale:
Provas
Questão presente nas seguintes provas
O conhecimento sobre os sítios de metabolização presentes na estrutura de um determinado fármaco e sobre as transformações metabólicas que estão sujeitos permitem:
I. compreender a eficácia farmacológica dos fármacos e a biodisponibilidade.
II. antecipar potenciais efeitos secundários e/ou tóxicos, dependentes da formação de metabólitos ativos.
III. planejar novos fármacos mais seguros e de posologia ajustada.
I. compreender a eficácia farmacológica dos fármacos e a biodisponibilidade.
II. antecipar potenciais efeitos secundários e/ou tóxicos, dependentes da formação de metabólitos ativos.
III. planejar novos fármacos mais seguros e de posologia ajustada.
Provas
Questão presente nas seguintes provas
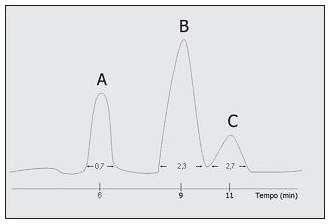
A qualidade de uma separação cromatográfica é medida pela resolução, que é o grau de afastamento entre dois picos eluidos próximos. As resoluções entre os picos A e B, e B e C, mostrados no cromatograma abaixo podem ser calculadas baseado nos valores de tempo de retenção e largura de pico:

Provas
Questão presente nas seguintes provas
Para o registro de medicamentos fitoterápicos (ou produtos) com indicação de uso tópico, deve-se:
I. apresentar, facultativamente, resultados de ensaios de toxicidade aguda oral, visando prever o que aconteceria em casos de uso indevido (intoxicação por ingestão acidental) do medicamento.
II. apresentar obrigatoriamente ensaios de toxicidade aguda oral, segundo disposto na RE 90/04.
III. apresentar estudos que comprovem que a absorção sistêmica é negligenciável, informando que o produto não deve ser usado em casos de pele lesionada.
Assinale:
I. apresentar, facultativamente, resultados de ensaios de toxicidade aguda oral, visando prever o que aconteceria em casos de uso indevido (intoxicação por ingestão acidental) do medicamento.
II. apresentar obrigatoriamente ensaios de toxicidade aguda oral, segundo disposto na RE 90/04.
III. apresentar estudos que comprovem que a absorção sistêmica é negligenciável, informando que o produto não deve ser usado em casos de pele lesionada.
Assinale:
Provas
Questão presente nas seguintes provas
As interações entre biomoléculas são sempre:
Provas
Questão presente nas seguintes provas
O fármaco A apresenta afinidade (Ki= 30 nM) e atividade intrínseca (I= 1) diferente do fármaco B (Ki= 0,15 ?M; I= - 1). Considerando os valores de Ki e I, pode afirmar-se que:
I. O fármaco B é um agonista inverso.
II. O fármaco A é um agonista total.
III. O fármaco A apresenta potência 50 vezes maior que o fármaco B.
I. O fármaco B é um agonista inverso.
II. O fármaco A é um agonista total.
III. O fármaco A apresenta potência 50 vezes maior que o fármaco B.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container