Foram encontradas 2.943 questões.
Analise o esquema que mostra um sistema genérico usado para cromotografia líquida de alta eficiência (CLAE ou HPCL – High Performance Liquid Chromatography), a qual, independente do fabricante e do modelo atual, apresenta os seguintes princípios:
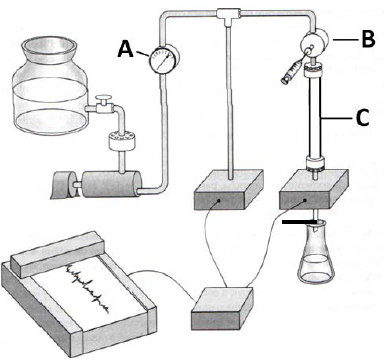
Os componentes identificados pelas letras A, B e C são, respectivamente,
Provas
A figura a seguir apresenta um aparelho típico usado na destilação simples, cujos componentes estão destacados e identificados por letras. Observe.
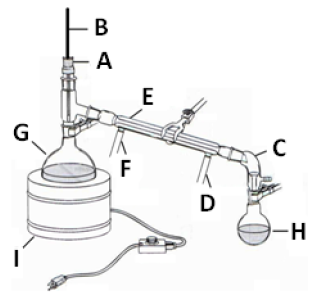
Com base na figura anterior, é INCORRETO afirmar que o(a)
Provas
Os compostos binários, cujo elemento mais eletronegativo é o oxigênio, classificam-se em: óxidos, peróxidos e superóxidos, em função do valor no número de oxidação (Nox) do átomo de oxigênio. Assinale a alternativa que apresenta somente peróxidos.
Provas
Para facilitar o trabalho dos químicos, os compostos químicos foram dividos em diversas classes ou funções. Duas funções importantíssimas são os ácidos e as bases. Historicamente, os conceitos que definem os ácidos e as bases mudaram conforme a evolução dos conceitos e o entendimento da química. Diante do exposto, analise as afirmativas.
I. O sueco Svante Arrhenius recebeu o Prêmio Nobel de Química devido aos seus trabalhos de dissociação eletrolítica. Dentro destas teorias, tem-se as seguintes definições: “ácido é toda substância química que, em água, libera como cátion exclusivamente íons H+” e “base é toda substância química que, em água, libera como ânions exclusivamente íons H+”. Trata-se da teoria iônica.
II. Em 1923, Johannes Nicolaus Bronsted e Thomas Martin Lowry propuseram, independente, a teoria ácido-base de Bronsted-Lowry. Para eles, “ácido é toda substância que libera íons H+” e “base é toda substância que recebe (ou aceita) íons H+”. Trata-se da teoria protônica.
III. Gilbert Newton Lewis, em 1916, foi um dos grandes responsáveis pelas explicações adequadas sobre as ligações covalentes, a partir do estudo do comportamento dos elétrons. Para Lewis, “ácido é toda substância capaz de aceitar (ou receber pares de elétrons) pares de elétrons de outra substância” e “base é toda substância capaz de doar (ou ceder pares de elétrons) pares de elétrons para outra substância”. Trata-se da teoria eletrônica.
Está(ão) correta(s) a(s) afirmativa(s)
Provas
Os compostos orgânicos, dependendo da função, podem apresentar características de ácidos. Evidentemente, são ácidos muito mais fracos que os ácidos inorgânicos. Assinale a alternativa que apresenta apenas compostos orgânicos com características ácidas.
Provas
Sobre as ligações químicas, assinale a afirmativa INCORRETA.
Provas
Propriedades periódicas são aquelas definidas na tabela periódica, conforme a variação do número atômico (Z) dos elementos químicos. Sobre o tema, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A eletronegatividade diminui no período da esquerda para a direita e na família de baixo para cima.
( ) A eletroafinidade aumenta no período da esquerda para a direita e na família de cima para baixo.
( ) O potencial de ionização diminui no período da direita para a esquerda e na família de cima para baixo.
A sequência está correta em
Provas
Óxidos são compostos em que o elemento mais eletronegativo é o oxigênio com número de oxidação total e igual a – 2 (Nox = – 2). De acordo com o comportamento dos óxidos frente a outras substâncias, eles podem ser classificados em: ácidos, básicos ou anfotéricos. Assinale a alternativa que apresenta um óxido ácido.
Provas
Sobre as ligações químicas, analise as afirmativas.
I. A característica principal das ligações iônicas é a grande diferença de eletronegatividade entre os átomos. Um átomo deve ter baixa energia de ionização e o outro uma elevada afinidade eletrônica.
II. A atração eletrostática entre os íons na ligação iônica é a força mais significativa da estabilização da ligação.
III. A baixa energia de ionização necessária para uma ligação iônica é característica dos metais. A alta energia de afinidade eletrônica, que também é necessária para uma ligação iônica, é uma característica dos elementos químicos não metálicos, que necessitam de um, dois ou três elétrons para completar suas camadas de valência.
Está(ão) correta(s) a(s) afirmativa(s)
Provas
No laboratório de química orgânica são realizados, constantemente, diversos processos químicos. Analise os dois processos que representam duas reações orgânicas muito comuns:
Processo 1
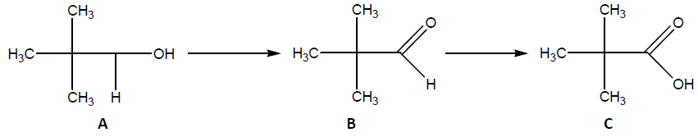
Processo 2
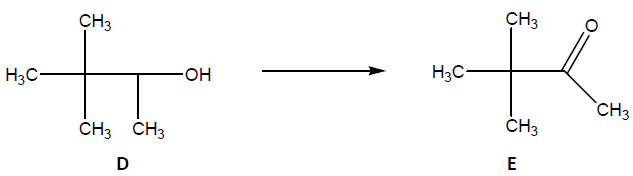
Diante do exposto, é INCORRETO afirmar que o composto
Provas
Caderno Container