Foram encontradas 60 questões.
O ácido sulfúrico pode ser produzido a partir de diversas fontes de enxofre. Uma dessas fontes é o mineral pirita (FeS2) que passa por um processo conhecido como ustulação. A ustulação consiste em aquecer o mineral sulfetado a altas temperaturas, na presença de oxigênio, o que leva à produção de dióxido de enxofre (SO2). O dióxido de enxofre é então oxidado a trióxido de enxofre (SO3), na presença de catalisador, o qual é absorvido em água para a produção de ácido sulfúrico.
O óxido metálico obtido segue para as rotas seguintes de tratamento. Para a pirita, a etapa de ustulação até a de produção de ácido sulfúrico pode ser representada pelas seguintes equações químicas.
!$ 4 FeS_{2(s)} + 11O_{2(g)} \underset { \rightarrow } {\triangle} 2\,Fe_2 O_{3(s)} + 8SO_{2(g)} !$
!$ SO_{2(g)} + 0,5O_{2(g)} \underset{ \longrightarrow} { (V_2\,O_5)} SO_{3(g)} !$
!$ SO_{3(g)} + H_2 O_{(l)} \rightarrow H_2 SO_{4(aq)} !$
Dados: FeS2 = 120g/mol; Fe2O3 = 160g/mol; O2 = 32g/mol; SO2 = 64g/mol; SO3 =80g/mol; H2O = 18g/mol; H2SO4 = 98g/mol
Dado que o mineral pirita é composto por 47% de ferro e 53% de enxofre, em massa, uma empresa que produz 20.000 toneladas por mês de ácido sulfúrico, utilizando um material composto por 70% de pirita e 30% de impurezas. Por mês, a quantidade, em toneladas, de pirita impura consumida pela empresa
Provas
Catalisadores são substâncias que diminuem a energia de ativação de uma dada reação, sem alterar quais são os produtos formados ou a estequimetria da reação. Imagine que você esteja produzindo N2 e H2 a partir da decomposição da amônia.
!$ NH_{3(g)} \rightleftarrows { \large 1 \over 2} N_{2(g)} + { \large 3 \over 2} H_{2(g)}\,\,\,\triangle H= 46 { \large Kj \over mol} !$
A energia de ativação para essa reação é igual a 150kJ/mol, em um meio homogêneo, na ausência de um catalisador, e cai para 87kJ/mol na presença de um catalisador sólido específico
Considere as seguintes afirmações sobre a decomposição da amônia.
I. A velocidade da reação na superfície do catalisador depende da área superficial do catalisador.
II. As constantes de velocidade para os dois casos (sem e com catalisador) são iguais.
III. A velocidade no meio homogêneo é igual a da mesma reação no meio heterogêneo.
Está correto o que se afirma em:
Provas

Provas
O saturador adiabático é um equipamento utilizado para umidificar o ar em um processo industrial. Esse equipamento consiste de uma câmara contendo água no estado líquido sobre a qual passa uma corrente de ar. A água evapora adiabaticamente e, assim, o ar que entra seco no equipamento, sai umidificado. Considerando um saturador adiabático que possua uma câmara que comporta 5.000cm3 de água e com uma altura h de 500cm. Ar seco entra no equipamento e, após umidifcado, sai com água a uma concentração igual a 50% da saturação, a uma velocidade constante, sem que haja perturbações na superfície da água. O nível da água é mantida constante devido ao bombeamento de 20cm3.h-1 de água para dentro da câmara. O sistema opera a 25°C (298K) e 101kPa. O coeficiente de difusão da água no ar é igual a 900cm2.h-1, a densidade da água líquida é 1,0g.cm-3, a massa molar da água é 18g.mol-1 e a pressão de vapor da água 3,17kPa.
A constante dos gases pode ser admitida como 8314kPa.cm3.mol-1.K-1.

Fonte: Arquivo da Banca Elaboradora.
O fluxo de água que evapora é igual a
Provas

Provas
Provas
Provas
Provas
O dono de uma empresa verificou que aumentaria muito seus lucros caso passasse a produzir uma de suas matérias-primas, ao invés de comprá-la, apesar do investimento inicial necessário. Essa matéria-prima é produzida a partir da decomposição de uma dada substância A. Ele desejava conseguir uma conversão de85% utilizando até três reatores, com o menor volume total possível. Primeiramente, ele pediu a um de seus funcionários que estudasse como a velocidade da reação se correlacionava com a conversão do reagente A.
O funcionário apresentou a tabela a seguir, em que a variação do número de moles do reagente A (dNA/dt) está expressa em mol/s.
| Conversão de A | 0 | 0,1 | 0,2 | 0,3 | 0,4 | 0,5 | 0,6 | 0,7 | 0,8 | 0,9 |
| dNA/dt (mol/s) | 0,300 | 0,326 | 0,355 | 0,388 | 0,425 | 0,462 | 0,492 | 0,497 | 0,441 | 0,275 |
A partir desses dados, foi possível desenhar o gráfico a seguir.
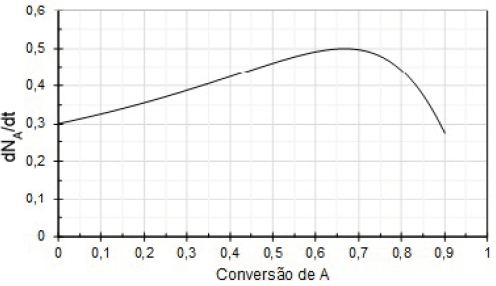
Fonte: Arquivo da Banca Elaboradora.
Assim, o dono da empresa verificou que, para atender suas condições, o ideal seria utilizar um
Provas
Quando se deseja estudar a distribuição de tamanho de partículas, é necessário, inicialmente, medir os tamanhos das partículas. A técnica mais utilizada para isso é o peneiramento, que consiste no empilhamento de peneiras que possuem malhas de aberturas diferentes, sendo as de malhas mais largas colocadas no topo e as de malhas mais estreitas colocadas no fundo. No estudo de distribuição do tamanho de partículas, não se caracteriza como uma dificuldade da técnica de peneiramento,
Provas
Caderno Container