Foram encontradas 1.800 questões.
A obtenção do ferro se dá na reação entre o minério de ferro, o óxido de ferro II (MM = 71,8 g/mol) e o monóxido de carbono, de acordo com a seguinte equação:
FeO(s) + CO(g) → Fe(s) + CO2(g)
Considerando as equações termoquímicas de outros minérios de ferro, como a hematita, a magnetita e a wusita, a entalpia de obtenção do ferro, a partir 215,4 g de óxido de ferro, é igual a:
Fe2O3(s) + 3CO(g) → 2 Fe(s) + CO2(g)
!$ \Delta H_1 = -25 kJ/mol !$
3FeO(s) + CO2(g) → Fe3O4(s) + CO(g)
!$ \Delta H_2 = -36 kJ/mol !$
2 Fe3O4(s) + CO2(g) → 3 Fe2O3(s) + CO(g)
!$ \Delta H_3 = +47 kJ/mol !$
Provas
Ao planejar uma síntese orgânica, é necessário conhecer as propriedades físico-químicas dos reagentes envolvidos na reação, para propor a melhor rota e os mecanismos. Uma dessas propriedades é a basicidade dos compostos, que indica a habilidade de a molécula receber o próton e formar um produto estável. Dentre as moléculas a seguir, aquela que forma o produto mais estável em uma reação ácido base é a:
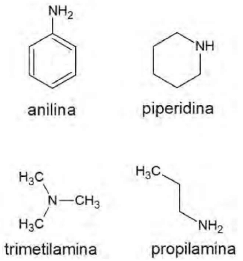
Provas
As sucessivas ionizações no nitrogênio e suas respectivas energias de ionização estão representadas no gráfico abaixo:
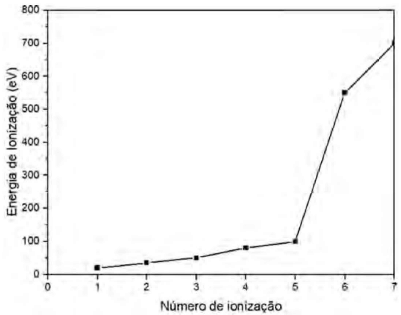
A grande variação de energia que ocorre entre a quinta ionização e a sexta ionização é devido:
Provas
A Morina é um substrato orgânico modelo, utilizado para avaliar a capacidade alvejante em processos de branqueamento. Essa avaliação pode ser feita através do decaimento de sua banda em 390 nm, em uma cu beta de 2 mL, em um espectrofotômetro. A concentração ideal da Morina na cubeta é de 5 x 10-5 mol L-1 para evitar o limite máximo de detecção dos aparelhos. Se 200 µL provenientes de uma solução mãe estocada em um balão volumétrico de 100 mL são adicionadas à cubeta (volume total 2 mL), a massa necessária de Morina para preparar a solução mãe, considerando a concentração final ideal, é de:
(Massa Molar Morina = 302,23 g/mol)
Provas
O decaimento radioativo é acompanhado por uma grande variação de energia, muito maior do que uma reação química e, por isso, é considerado uma fonte de energia eficiente. O decaimento de 1 mol de Urânio-238, conforme a equação abaixo, é 50 vezes maior que a queima do metano:
!$ ^{238}_{92}U \rightarrow ^{234}_{90}Th + ^4_2He !$
Considerando a velocidade da luz igual a 3,0 x 108 m s-1 e as massas dos núcleos de urânio iguais a 238,0003, de tório iguais a 233,9942 e de hélio iguais a 4,0015, a energia liberada nessa reação é de:
Provas
Uma pilha pode ser construída com dois eletrodos de hidrogênio: o primeiro com 1,00 atm de gás hidrogênio e o segundo com uma solução ácida de pH = 2,0. A 298 K, observa-se que a corrente elétrica flui do primeiro eletrodo para o segundo, e o potencial da célula é de:
(Dados: R=8,314J mol-1 K-1; F=96500sAmol-1)
Provas
A decomposição térmica do ciclopropano ocorre a 500°C, formando o propeno. A velocidade dessa reação ocorre por um mecanismo de primeira ordem. Se a constante de velocidade dessa reação, nessa temperatura, é de 7 x 10-4 s-1, o tempo necessário para decompor 3 x 103 em 2,1 x 10-3 mol dm-3 é de aproximadamente:
(Dados: In = 2,3 log; log 2 = 0,3; log 3 = 0,47; log 5 = 0,69; log7=0,84)
Provas
O biomimético [VO(acac)(bmimapy)]!$ C\ell O_4 !$ é um complexo sintetizado a partir do bis(acetilacetonato) de vanadila com o ligante bmimapy e pode ser caracterizado através da comparação de seus espectros no UV-vis, conforme representado a seguir:
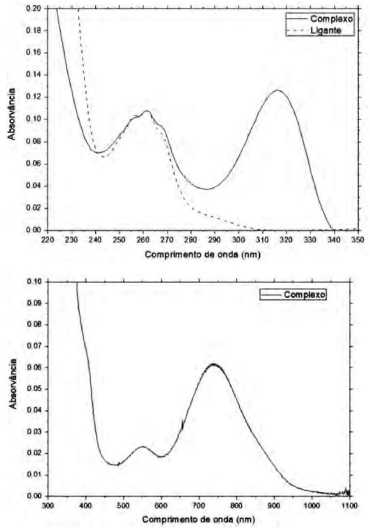
É possível observar novas bandas em 320 nm e em 740 nm quando se compara o ligante com o complexo. Essas bandas são respectivamente:
Provas
O limoneno, produto natural encontrado na casca da laranja, é um composto com alto valor agregado, com diversas aplicações na indústria farmacêutica, e está representado a seguir:

Durante a síntese de uns desses materiais de interesse, o limoneno sofre hidrogenação catalítica, com o intuito de eliminar todas as suas insaturações. Em CNTP, o volume de hidrogênio necessário para obter o produto de interesse a partir de 8,5 9 de limoneno (teor de pureza de 80%) é de:
(Dados: MM limoneno = 136 g mol-1 ; Volume molar em CNTP = 22,4 L)
Provas
O brometo de benzila ou !$ \alpha !$-bromotolueno é um agente lacrimogênio que pode ser produzido a partir do benzeno em uma sequência de reações conforme o esquema simplificado a seguir:
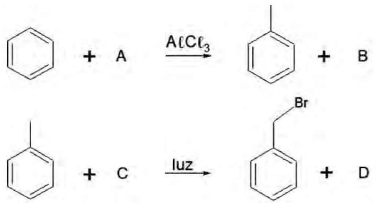
Os reagentes A e C que completam o esquema reacional são:
Provas
Caderno Container