O diagrama p x V (pressão versus volume), abaixo, apresenta uma transformação gasosa cíclica A\( \rightarrow \) B\( \rightarrow \) C\( \rightarrow \) D \( \rightarrow \)A sofrida por \( n \) moles de um gás ideal. As transformações A\( \rightarrow \) B e C \( \rightarrow \)D são isotérmicas cujas temperaturas absolutas valem, respectivamente, 2T e T.
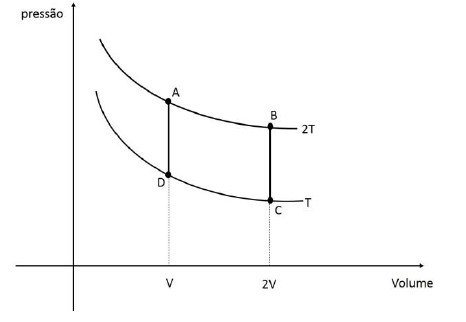
Considerando R a constante de Clayperon e \( ln \) o logaritmo natural, popularmente denominado de logaritmo neperiano, é correto afirmar que, nessa transformação, o gás foi submetido a um trabalho igual a