Uma das maneiras de enunciar a 1ª Lei da Termodinâmica
é: “a variação da energia do sistema tem que ser igual
à energia transferida através das suas fronteiras com as
vizinhanças”. Assim, para um sistema fechado sem reação química, ela pode ser expressa pela equação:
∆U + ∆Ek
+ ∆Ep
= Q + W
Sendo: ∆U: variação da energia interna (propriedade termodinâmica
da substância); ∆Ek
e ∆Ep
: variações das
energias cinética e potencial, respectivamente; Q: calor;
W: trabalho que acompanha a variação no volume do sistema.
Aplicando-se a 1ª Lei da Termodinâmica e conhecendo-se
as propriedades termodinâmicas da água (Tabela
a seguir), pode-se estimar a quantidade de trabalho
realizado e o calor necessário para uma massa de
1,0 kg de água líquida a 100 ºC, contida em um cilindro
por um êmbolo a uma pressão de 0,7 MPa, que é aquecida
lentamente até ocupar todo o volume do cilindro.
Neste momento, o sistema é uma mistura de líquido mais
vapor. Transfere-se, então, mais calor ao sistema, até a
água tornar-se vapor saturado a 180 ºC.
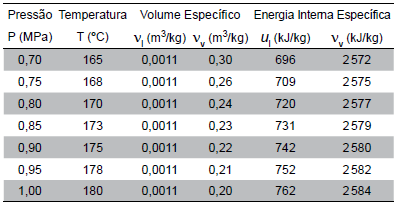
Propriedades Termodinâmicas da Água Saturada