Foram encontradas 36.327 questões.
O tetracloreto de titânio IV tem sido usado para se "escrever no céu" com aviões em alguns espetáculos aéreos e na fabricação de bombas de fumaça. Assim, assinale a opçâo que apresenta a fórmula correta do tetracloreto de titânio IV.
Provas
Com base nos dados da tabela abaixo, assinale a opção correta.
| Átomo | Símbolo | Prótons | Elétrons | Néutrons |
| I | \( ^{18}_8O \) | 8 | 8 | 10 |
| II | \( ^{19}_9F \) | 9 | 9 | 10 |
| III | \( ^{20}_{10}N \) | 10 | 10 | 10 |
Provas
Observe a tabela abaixo.
|
Compostos e alaumas de suas aolicacões |
||
|
Composto |
Fórmula |
Aplicação |
| I | ZnO | Maquiagem |
| II | KCl | Adubação |
Com base nas informações da tabela acima, assinale a opção que apresenta as funções inorgânicas dos compostos I e II.
Provas
Assinale a opção que apresenta corretamente uma reação química de síntese.
Provas
Coloque F (falso) ou V (verdadeiro) nas afirmativas abaixo, em relação á posição de alguns elementos químicos na tabela periódica, assinalando a seguir a opção correta.
( ) O elemento do grupo dos halogênios que está no mesmo período do metal alcalino com 19 prótons é o bromo (Br).
( ) O elemento oxigênio (O) está no grupo dos gases nobres.
( ) Os elementos químicos estrôncio (Sr) e silício (Si) estão no grupo dos calcogênios.
( ) O elemento níquel (Ni) no grupo 10 da tabela periódica é um elemento de transição.
Provas
Uma das etapas da fermentação láctea consiste na transformação de ácido pirúvico em ácido láctico, pela reação representada pela equação:
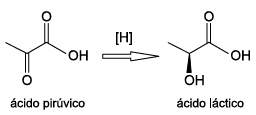
Na transformação de ácido pirúvico em ácido láctico ocorre do grupo de um composto opticamente , formando um composto opticamente .
As lacunas do texto são preenchidas, respectivamente, por:
Provas
Água de cal é o nome dado à solução aquosa saturada de cal hidratada [hidróxido de cálcio, Ca(OH)2]. A concentração dessa solução saturada a 20 ºC é de 1,7 g/L. A partir desse dado, estima-se que o valor da constante do produto de solubilidade em água (Kps) nessa temperatura é próximo de
Provas
Analise a tabela, que apresenta valores da entalpia padrão de combustão completa (ΔcH0) de três substâncias diferentes.
|
Substância |
Fórmula | Produtos da combustão completa |
ΔcH0 de combustão completa (kJ/mol) |
|
Ácido acético |
C2H4O2 (\( \ell \)) | CO2 (g) e H2O (l) |
– 874 |
|
Carbono |
C (s,grafita) | CO2 (g) |
– 394 |
|
Hidrogênio |
H2 (g) | H2O (l) |
– 286 |
A partir desses valores de entalpia de combustão, é possível calcular a entalpia de formação do ácido acético, que é, em kJ/mol, igual a
Provas
A montagem de laboratório ilustrada na figura destina-se à coleta e medida do volume de produto gasoso gerado numa reação química.
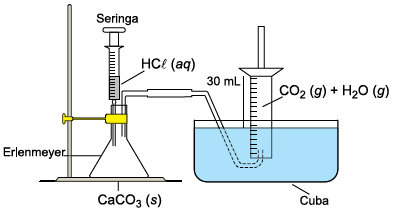
Em um experimento, envolvendo a produção de dióxido de carbono gasoso, CO2 (g), a partir da reação entre carbonato de cálcio, CaCO3 (s), e solução aquosa diluída de ácido clorídrico, HC\( \ell \) (aq), o líquido empregado para a coleta do gás foi a água acidulada. Um comprimido de CaCO3 foi triturado e uma porção do pó resultante foi colocada no erlenmeyer da montagem e posta para reagir com solução de HC\( \ell \), adicionada a partir da seringa da montagem. Após a reação, o produto gasoso coletado no cilindro graduado teve seu volume determinado, sendo igual a 30 mL. Sabe-se que o produto gasoso recolhido é uma mistura de dióxido de carbono gasoso e vapor de água.
Considerando que o experimento foi realizado sob pressão atmosférica de 726,7 mmHg e temperatura de 27 ºC, que a pressão de vapor da água a 27 ºC é igual a 26,7 mmHg e que a constante universal dos gases, R, é igual a 62,3 mmHg · L · mol–1 · K–1, a massa de carbonato de cálcio que reagiu na produção de dióxido de carbono gasoso foi de, aproximadamente,
Provas
O sistema Li/MnO2 é o exemplo mais representativo das pilhas primárias (de uso único) de lítio.

(www.smartkits.com.br)
Essas pilhas empregam eletrólitos dissolvidos em solventes não aquosos, em recipientes selados.
O processo de descarga dessa pilha envolve a reação 4Li + MnO2 → 2Li2O + Mn
Essa pilha fornece uma diferença de potencial (voltagem) em torno de 3,0 V à temperatura ambiente, mas mostra excelente desempenho em temperaturas superiores.
A grande vantagem das pilhas à base de lítio é a ausência de metais pesados reconhecidamente danosos ao meio ambiente, como mercúrio, cádmio e chumbo. Porém, os perigos relativos à pilha Li/MnO2 são de outra natureza, estando relacionados ao seu descarte e reciclagem. Após a corrosão do invólucro externo, é liberado o solvente não aquoso, inflamável e tóxico. O lítio metálico não reagido, em contato com água e umidade do ar, desprende calor e gás inflamável (hidrogênio), podendo levar à ignição do produto descartado. Por isso, a presença de voltagem residual nesse resíduo é um problema, pois significa a presença de lítio metálico.
As características listadas para a pilha de lítio tornam a disposição final inadequada e até mesmo a reciclagem uma operação de risco, pela possibilidade de fogo e explosão.
(Jéssica Frontino Paulino et al. “Processamento de pilhas Li/MnO2 usadas”. Quim. Nova, vol. 30, 2007. Adaptado.)
Para tornar a reciclagem dessa pilha mais segura, o ideal seria o seu descarregamento completo antes do descarte, evitando assim a
Provas
Caderno Container