Foram encontradas 36.242 questões.
Complexos são termodinamicamente mais estáveis quando formados por agentes quelantes, que são ligantes polidentados, em comparação a um número equivalente de ligantes monodentados. Um exemplo importante na medicina é a aplicação de agentes quelantes para a remoção seletiva de íons metálicos tóxicos como Hg2+ e Pb2+, preservando os metais biologicamente importantes.
As figuras abaixo mostram alguns exemplos de ligantes quelantes:
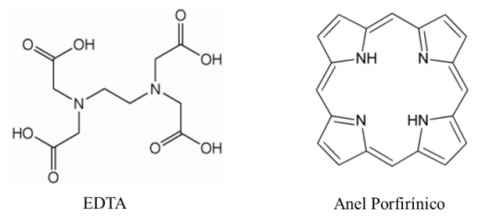
Com base na estabilidade dos íons complexos e agentes quelantes, analise as afirmações abaixo:
I. A constante de formação do quelato é extremamente alta quando comparada a ligantes monodentado de mesma natureza. Isso se deve à energia livre de Gibbs ser mais negativa, sendo governada pelo efeito entálpico em detrimento ao efeito entrópico.
II. O EDTA é um ácido poliprótico cuja estrutura pode ser dada pela fórmula H4Y, um quelante hexadentado muito utilizado na indústria de alimentos e na medicina. O EDTA forma complexos octaédricos com o centro metálico.
III. Quelatos com íons metálicos das séries mais elevadas tendem a ser mais lábeis, o que pode explicar a preferência de ligantes quelantes por íons como Hg2++ e Pb2+ .
IV. Os anéis porfirínicos possuem 4 pontos de coordenação e formam uma classe de ligantes quelantes, responsável, por exemplo, pela estabilidade do grupo heme, onde o centro metálico é um íon de ferro.
Assinale a alternativa com as afirmações CORRETAS.
Provas
As funções inorgânicas são grupos de compostos inorgânicos que apresentam características semelhantes. Sobre os ácidos e as bases, presentes na classificação dos compostos inorgânicos, analise as premissas abaixo e marque V para verdadeira e F para falso.
( ) Os ácidos são capazes de se ionizar em meio aquoso, liberando uma certa quantidade de hidrogênios, formando o cátion H+.
( ) Os ácidos podem apresentar um forte grau de ionização, superior a 50%, como por exemplooH2S e HCN.
( ) As bases são classificadas de acordo com o número de hidroxilas (OH) liberadas em solução.
( ) As bases compostas por metais alcalinos são insolúveis em água e as bases compostas por metais alcalinos-terrosos são pouco solúveis em água.
Assinale a alternativa correta.
Provas
Um dos modelos atômicos propostos, para estudar o átomo e suas partículas elementares, sugere que o átomo apresenta o aspecto de um planetário. De acordo com esse modelo, os elétrons giram em torno do núcleo, na qual é formado por prótons e nêutrons, de forma semelhante aos planetas que giram ao redor do sol. De acordo com a descrição dessa teoria, esse modelo atômico foi proposto por qual pesquisador:
Provas
Em relação à composição do ar atmosférico, analise as proposições e marque V para verdadeira e F para falso.
( ) O ar atmosférico que envolve o planeta Terra é uma mistura de gases, fuligem, vapor d’água, produtos químicos e partículas suspensas.
( ) Os elementos que compõem o ar são essencialmente formados pelo gás nitrogênio(78%),oxigênio (21%), gás carbônico (0,03%), enxofre (0,94%) dentre outros.
( ) O ar é composto de matéria, afinal é formado por gases, portanto tem massa e ocupa lugar no espaço.
( ) A medida que aumenta a altitude, diminui a pressão atmosférica, pois tem menos ar acima.
Marque a alternativa correta de acordo com as proposições consideradas verdadeiras ou falsas.
Provas
Provas
Observe as seguintes distribuições eletrônicas:
A=1s2 2s2 2p6 3s
B = 1s2 2s2 2p6 3s2 3p5
C = 1s2 2s2 2p6 3s2 3p4
D= 1s2 2s2 2p6 3s2 3p6 4s2
Assinale a alternativa correta.
Provas
Provas
Analise as afirmativas abaixo sobre a tabela periódica e seus elementos:
I - Os metais alcalinos e alcalinos terrosos, grupos 1 e 2, respectivamente, são os únicos metais que apresentam número de oxidação fixo.
II – A molécula de água, ao saturar, produz o cátion hidrônio e o cálcio. Por essa razão, nessa reação de hidrogenação, além do composto orgânico, o outro reagente é a água. Assim, um dos carbonos, onde ocorre a cisão (quebra da ligação sigma ou pi, como visto anteriormente), recebe o cátion de hidrônio, e o outro recebe o ânion de hidróxido".
III - A temperatura de fusão dos metais dos grupos 1 e 2 diminui com o aumento do período da tabela periódica.
IV - "Durante uma reação de oxirredução, ocorre o rompimento de uma ou mais ligações pi, ou de uma ligação sigma (no caso exclusivo de um ciclano), fazendo com que surjam duas ou mais valências livres (sítios de ligação) nos carbonos envolvidos".
V - Apesar de possuírem a última camada de valência completa, alguns elementos do grupo 18 podem formar compostos com átomos bastante eletronegativos, como F e O.
Assinale:
Provas
Provas
Analise as afirmativas abaixo e dê valores Verdadeiro (V) ou Falso (F).
( ) Na reação de adição, além do composto orgânico, o outro reagente é o gás carbônico. Em cada um dos carbonos, onde ocorre a cisão (quebra da ligação sigma ou pi, como visto anteriormente), haverá a ligação de um átomo de carbono referente à quantidade de ligações rompidas.
( ) Um halogenidreto é putrefação, formado por um átomo de oxigênio e um átomo de halogênio, como o gás clorídrico, o ácido fluorídrico (HF), ácido bromídrico (HBr), ácido iodídrico (HI).
( ) Eletronegatividade é a capacidade que um átomo possui de atrair os elétrons envolvidos em uma ligação química. Os valores de eletronegatividade são baseados em outras propriedades dos átomos, inclusive a energia de ionização, portanto, elementos com baixa energia de ionização exibirão baixa eletronegatividade.
( ) O raio atômico representa a medida entre o núcleo e a camada de valência do átomo. Os raios atômicos diminuem em uma mesma família da tabela periódica e a diminuição é bastante pronunciado para os metais alcalinos. Ele é inversamente proporcional à eletronegatividade porque quanto ´menor for a força que o núcleo atrai a eletrosfera, maior é o raio.
Assinale a alternativa que apresenta a sequência correta.
Provas
Caderno Container