Foram encontradas 36.167 questões.
Todos os símbolos a seguir estão relacionados a perigo para substâncias químicas.
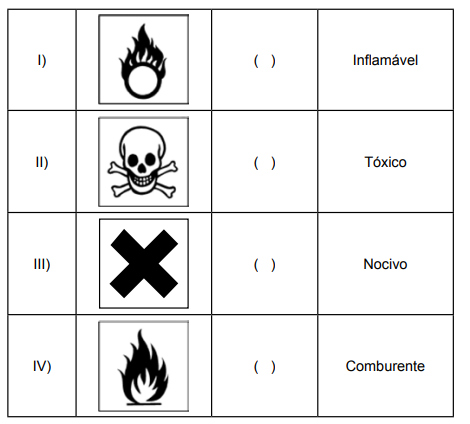
Disponível em: https://ec.europa.eu/taxation_customs/dds2/SAMANCTA/PT/Safety/SymbolsOfHazard_PT.htm. Acesso em: 01 mai. 2025.
Assinale a alternativa que relaciona corretamente o pictograma a seu significado.

Disponível em: https://ec.europa.eu/taxation_customs/dds2/SAMANCTA/PT/Safety/SymbolsOfHazard_PT.htm. Acesso em: 01 mai. 2025.
Assinale a alternativa que relaciona corretamente o pictograma a seu significado.
Provas
Questão presente nas seguintes provas
Considere desvios das leituras de pH, observados pela técnica de potenciometria, nas seguintes
curvas:

SKOOG, D.; WEST, D.; HOLLER, F. J. e CROUCH, S; Fundamentos de Química Analítica; (2014), p. 548.
Com base nessas informações, constata-se que se trata de

SKOOG, D.; WEST, D.; HOLLER, F. J. e CROUCH, S; Fundamentos de Química Analítica; (2014), p. 548.
Com base nessas informações, constata-se que se trata de
Provas
Questão presente nas seguintes provas
O potencial hidrogeniônico (pH) é uma medida da acidez ou alcalinidade de uma
solução. Assinale a única alternativa que apresenta um pH ácido.
Provas
Questão presente nas seguintes provas
O potencial hidrogeniônico (pH) é uma medida da acidez ou alcalinidade de uma
solução. Assinale a alternativa que aponta a classificação de uma solução com pH = 4,75.
Provas
Questão presente nas seguintes provas
Em uma aula prática de Ciências, os alunos realizaram um experimento com três substâncias diferentes: cloreto de sódio
(sal de cozinha), sacarose (açúcar) e cobre metálico. Eles observaram o comportamento dessas substâncias ao serem colocadas
na água e ao conduzir corrente elétrica. O sal se dissolveu e conduziu eletricidade, o açúcar se dissolveu, mas não conduziu
eletricidade, e o cobre não se dissolveu, mas conduziu eletricidade quando ligado a uma bateria. Com base nas observações e nos
conhecimentos sobre tipos de ligações químicas, identifique a alternativa correta.
Provas
Questão presente nas seguintes provas
A respeito dos métodos de separação de misturas, é correto
afirmar que
Provas
Questão presente nas seguintes provas
Uma empresa contatou a central analítica para determinar a composição de um material. A amostra em questão, de
massa 0,648 g, é formada por um sal de oxalato anidro, cuja composição é do tipo MC2O4 (M é um metal a ser
determinado). Essa amostra foi submetida à calcinação ao ar, gerando 0,348 g de resíduo sólido. O resultado da análise
indicou que a composição do resíduo é M3O4.
Dados:
Massa molar (g mol–1): C = 12, O = 16, Sc = 45, Ti = 48, Fe = 56, Co = 59, Ga = 70
O metal (M) presente no sal é:
Dados:
Massa molar (g mol–1): C = 12, O = 16, Sc = 45, Ti = 48, Fe = 56, Co = 59, Ga = 70
O metal (M) presente no sal é:
Provas
Questão presente nas seguintes provas
Durante um experimento de bioquímica, verificou-se que a solução-tampão pH 6,8 havia acabado. Assim, decidiu-se
preparar uma nova solução tampão, a partir de 200 mL de uma solução-estoque 0,1 mol L−1 de mono-hidrogenofosfato
de sódio (Na2HPO4), na qual será adicionado o sal di-hidrogenofosfato de sódio di-hidratado (NaH2PO4ꞏ2H2O) para
ajustar o pH.
Dados:
Massa molar (g mol–1): Na = 23, H = 1, P = 31, O = 16 H2PO4 – + H2O ⇌ HPO4 2–+ H3O+ Ka = 6,3 x 10–8 log 6,3 x 10–8 = –7,2; log 1,6 x 10–7 = −6,8; log 0,4 = −0,4
Qual é a massa, em gramas, do sal que deve ser adicionada?
Dados:
Massa molar (g mol–1): Na = 23, H = 1, P = 31, O = 16 H2PO4 – + H2O ⇌ HPO4 2–+ H3O+ Ka = 6,3 x 10–8 log 6,3 x 10–8 = –7,2; log 1,6 x 10–7 = −6,8; log 0,4 = −0,4
Qual é a massa, em gramas, do sal que deve ser adicionada?
Provas
Questão presente nas seguintes provas
O peróxido de éter etílico (ou 1-etoxietil hidroperóxido), de massa molar igual a 106 g mol─1, se forma lentamente
quando o éter etílico é exposto à luz e ao ar, em temperatura ambiente. Esse peróxido e seus produtos de condensação
aparentam ser um líquido ou mesmo cristais que se depositam no fundo do frasco e podem causar explosões por
simples choque ou agitação do frasco, o que torna o armazenamento do éter muito perigoso. Pode-se considerar que
a reação de decomposição desse peróxido forma etanol e formaldeído.
Dados: ∆f H0 / kJ mol─1: 1-etoxietil hidroperóxido = –547,8; etanol = –234,7; formaldeído = –115,9.
Considerando que 1 g desse peróxido se forme no frasco, a quantidade de energia (em joules) envolvida na reação de decomposição será mais próxima de:
Dados: ∆f H0 / kJ mol─1: 1-etoxietil hidroperóxido = –547,8; etanol = –234,7; formaldeído = –115,9.
Considerando que 1 g desse peróxido se forme no frasco, a quantidade de energia (em joules) envolvida na reação de decomposição será mais próxima de:
Provas
Questão presente nas seguintes provas
Para análise de um lote de ácido ascórbico (H2A), de massa molar igual a 176 g mol−1, propôs-se a titulação com
permanganato de potássio. A reação, esquematizada a seguir, provoca a oxidação do ácido ascórbico, produzindo a
espécie A. No procedimento, utilizou-se uma solução padronizada 0,100 mol L−1 de permanganato para a titulação de
0,5 g de ácido ascórbico.
2 MnO4− + 5 H2A + 6 H+ → 2 Mn2+ + 5A + 8 H2O
Nessas condições, o volume estimado de titulante, em mL, é de:
2 MnO4− + 5 H2A + 6 H+ → 2 Mn2+ + 5A + 8 H2O
Nessas condições, o volume estimado de titulante, em mL, é de:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container