Foram encontradas 60 questões.
Tiossemicarbazonas (TSC) podem ser obtidas na forma direta a partir da reação quimiosseletiva de um aldeído e/ou cetona com uma tiossemicarbazida. Para tal, se fazem necessários a dispersão dos reagentes em meio alcoólico, a catálise
ácida e o aquecimento do solvente até a temperatura de ebulição, como mostrado no exemplo a seguir.
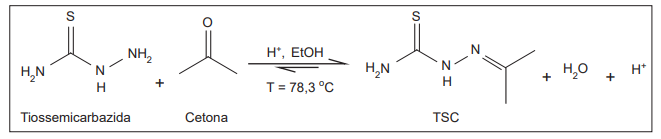
Considerando-se esse esquema reacional, a reação orgânica utilizada na obtenção da TSC é a

Considerando-se esse esquema reacional, a reação orgânica utilizada na obtenção da TSC é a
Provas
Questão presente nas seguintes provas
Considere as etapas termodinâmicas a seguir, pertencentes ao ciclo de Born-Haber, para a formação do LiF(s).
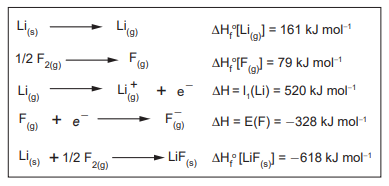
Nesse contexto, o valor aproximado da entalpia de rede (ΔHrede) para o LiF(s), em kJ mol-1 , é

Nesse contexto, o valor aproximado da entalpia de rede (ΔHrede) para o LiF(s), em kJ mol-1 , é
Provas
Questão presente nas seguintes provas
A coluna de Vigreux é adequada para ser utilizada na seguinte técnica de separação de misturas:
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Considerando-se que a fórmula molecular do metanotiol
é CH3
SH, os valores aproximados dos comprimentos de
ligação para C–H e S–H são 1,07 A
º
e 1,36 A
º
, respectivamente.
Nesse contexto, o valor aproximado do comprimento de ligação para C–S é
Dado raio covalente para H = 0,31 A
Nesse contexto, o valor aproximado do comprimento de ligação para C–S é
Dado raio covalente para H = 0,31 A
Provas
Questão presente nas seguintes provas
Ao adicionar o excesso de uma solução básica de
NaOH 6 mol L-1
e de H2
O2
3% v/v a uma solução aquosa desconhecida e, em seguida, aquecê-la, observou-
-se a formação de um precipitado marrom-avermelhado.
Após o resfriamento e a adição de uma solução ácida de
HCl 12 mol L-1
, obteve-se como resultado a completa
dissolução do sólido residual. Em seguida, adicionou-se
NH4
SCN 0,2 mol L-1
, levando à formação de um sólido de
cor vermelho-escura.
Nesse contexto, o resultado qualitativo obtido é a presença do íon
Nesse contexto, o resultado qualitativo obtido é a presença do íon
Provas
Questão presente nas seguintes provas
Niels Bohr realizou cálculos de energias associadas às
órbitas permitidas para o elétron no átomo de hidrogênio
isolado. As energias calculadas ajustam-se à fórmula
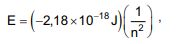
onde E é a energia da órbita permitida para um elétron no átomo de hidrogênio, em Joule, e n representa o número quântico principal que assume valores inteiros de 1, 2, 3, ... ∞ .
Dessa forma, com base nesse modelo atômico, para Bohr a(o)
onde E é a energia da órbita permitida para um elétron no átomo de hidrogênio, em Joule, e n representa o número quântico principal que assume valores inteiros de 1, 2, 3, ... ∞ .
Dessa forma, com base nesse modelo atômico, para Bohr a(o)
Provas
Questão presente nas seguintes provas
Numa curva de titulação volumétrica tradicional muitas
vezes é difícil visualizar o volume final da titulação. Uma
das estratégias é tratar os dados da titulação usando o
método de Gram.
Nessa abordagem, no caso de uma titulação redox monitorada com um eletrodo combinado, graficamente obtém-se a(o)
Nessa abordagem, no caso de uma titulação redox monitorada com um eletrodo combinado, graficamente obtém-se a(o)
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Na titulação argentométrica de 50,00 mL de solução de NaCl (2,0 × 10-2
mol L-1
), usou-se uma solução padronizada de
AgNO3
(4,0 × 10-2
mol L-1
) como representado na reação iônica a seguir.
Cl - (aq) + Ag+ (aq) → AgCl (s)
Após o ponto de equivalência, continuou-se adicionando 10,00 mL de excesso do agente titulante até que a concentração de íons em solução (ver equação a seguir) atingisse o equilíbrio.
AgCl (s) ⇄ Cl - (aq) + Ag+ (aq)
A concentração de Cl - na solução, em mol L-1 , será aproximadamente de
Cl - (aq) + Ag+ (aq) → AgCl (s)
Após o ponto de equivalência, continuou-se adicionando 10,00 mL de excesso do agente titulante até que a concentração de íons em solução (ver equação a seguir) atingisse o equilíbrio.
AgCl (s) ⇄ Cl - (aq) + Ag+ (aq)
A concentração de Cl - na solução, em mol L-1 , será aproximadamente de
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Um analista obteve os espectros de absorção molecular das substâncias: R-C=C-R, R-C=C-C=C-R e
R-C=C-C=C-C=C-R, onde R é um grupo comum às três substâncias. As substâncias estavam dissolvidas no mesmo
solvente e na mesma concentração em mol L-1
.
Em termos comparativos, em relação às outras duas substâncias, a banda espectral de
Em termos comparativos, em relação às outras duas substâncias, a banda espectral de
Provas
Questão presente nas seguintes provas
Um sistema coulométrico foi usado para a determinação de concentração hidrogeniônica (H+) de uma solução. Este consistia de duas meias-células, cada uma contendo um eletrodo de Pt e um eletrólito forte dissolvido, sendo as duas meias-
-células conectadas por ponte salina de KNO3
. Ao se acionar o sistema, no eletrodo de trabalho se formou gás O2
, e no
contra-eletrodo, o gás H2
. Adicionou-se vermelho de bromofenol à meia-célula que continha o eletrodo de trabalho, que
indicou, pela mudança de cor, o momento em que a amostra atingiu pH neutro. Nesse sistema, realizou-se uma análise de
100,00 mL de solução de pH 4,00, aplicando-se corrente constante de 50,0 mA.
Considerando-se esse sistema, verifica-se que
Dado F = 96.500 C mol-1
Dado F = 96.500 C mol-1
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container