Foram encontradas 1.170 questões.
- Química CinéticaRepresentação das Transformações Químicas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaGlicídios, Lipídios, Aminoácidos e Proteínas.
Uma transformação química milenar é a produção do etanol a
partir da fermentação de alimentos. Nesse processo, a levedura e
outros microrganismos fermentam a glicose (C6H12O6) em etanol
(C2H5OH) e CO2. Com relação à história da química e ao mundo
e suas transformações, julgue o item subsequente,
considerando 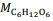 = 180 g/mol e
= 180 g/mol e 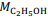 = 46 g/mol.
= 46 g/mol.
De acordo com a lei de Lavoisier, na reação de fermentação da glicose para produzir somente etanol e gás carbônico, em recipiente fechado, a massa de glicose consumida é igual à massa de etanol produzida, que é igual à massa de CO2 liberada.
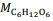 = 180 g/mol e
= 180 g/mol e 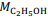 = 46 g/mol.
= 46 g/mol. De acordo com a lei de Lavoisier, na reação de fermentação da glicose para produzir somente etanol e gás carbônico, em recipiente fechado, a massa de glicose consumida é igual à massa de etanol produzida, que é igual à massa de CO2 liberada.
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Com relação a ligações químicas, eletronegatividade, repulsão de
pares eletrônicos e geometria molecular, julgue o item a seguir.
No íon NO3 − , há duas ligações mais longas e uma mais curta entre cada um dos átomos de oxigênio e o de nitrogênio.
No íon NO3 − , há duas ligações mais longas e uma mais curta entre cada um dos átomos de oxigênio e o de nitrogênio.
Provas
Questão presente nas seguintes provas
Com relação a ligações químicas, eletronegatividade, repulsão de
pares eletrônicos e geometria molecular, julgue o item a seguir.
Cátions e ânions estão mais fortemente ligados no NaCl que no KCl.
Cátions e ânions estão mais fortemente ligados no NaCl que no KCl.
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
Com relação a ligações químicas, eletronegatividade, repulsão de
pares eletrônicos e geometria molecular, julgue o item a seguir.
O composto SnCl3 apresenta geometria molecular tetraédrica.
O composto SnCl3 apresenta geometria molecular tetraédrica.
Provas
Questão presente nas seguintes provas
Com relação a ligações químicas, eletronegatividade, repulsão de
pares eletrônicos e geometria molecular, julgue o item a seguir.
Nas ligações covalentes entre átomos diferentes, os pares de elétrons são compartilhados igualmente.
Nas ligações covalentes entre átomos diferentes, os pares de elétrons são compartilhados igualmente.
Provas
Questão presente nas seguintes provas
Com relação a ligações químicas, eletronegatividade, repulsão de
pares eletrônicos e geometria molecular, julgue o item a seguir.
O comprimento da ligação entre o hidrogênio e o átomo de halogênio é maior no HI que no HF.
O comprimento da ligação entre o hidrogênio e o átomo de halogênio é maior no HI que no HF.
Provas
Questão presente nas seguintes provas
Com relação a ligações químicas, geometria molecular e teoria da
ligação de valência, julgue o item que se segue.
De acordo com a teoria de ligação de valência, o diagrama de orbitais para o átomo de Be, para formar orbitais híbridos no BeF2, está corretamente representado na figura a seguir.
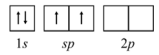
De acordo com a teoria de ligação de valência, o diagrama de orbitais para o átomo de Be, para formar orbitais híbridos no BeF2, está corretamente representado na figura a seguir.

Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- FundamentosTransformações: Estados Físicos e Fenômenos
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

No gráfico apresentado, os processos indicados pelas setas I e IV representam, respectivamente, os processos de vaporização e congelamento da referida substância.
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- FundamentosSubstâncias, Misturas e Processos de Separação
- FundamentosTransformações: Estados Físicos e Fenômenos
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

No gráfico apresentado, o segmento de curva entre os pontos O e T representa a curva de sublimação, que separa a fase sólida da fase gasosa, e cada ponto desse segmento é uma condição de equilíbrio entre o sólido e o gás.
Provas
Questão presente nas seguintes provas
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

Em geral, o desvio do comportamento ideal de um gás é mais evidenciado em pressões mais altas e em temperaturas mais baixas.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container