Foram encontradas 30 questões.
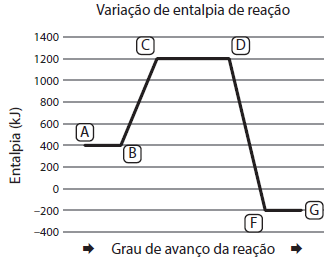
2. A energia de ativação desse processo é representada pelo segmento FG.
3. O perfil do gráfico permite afirmar que a reação direta representa uma reação de combustão.
4. A variação de entalpia (energia) de reação direta é de ΔH = – 600,00 kJ.
5. A reação inversa é exotérmica.
Provas
Analise as afirmativas a seguir:
1. A massa atômica de certo elemento que é apresentada na tabela periódica corresponde à média ponderal das massas atômicas dos seus isótopos naturais.
2. Os nêutrons são partículas subatômicas com carga positiva e têm aproximadamente amesma massa do elétron.
3. Os isótopos de um elemento têm o mesmo número atômico, mas diferentes números de massa.
4. Para um elemento neutro, a soma do número de prótons e de nêutrons corresponde ao seu número de massa.
5. A disposição dos elementos na tabela periódica está baseada no número atômico do elemento que corresponde à soma dos seus prótons e de seus elétrons.
Assinale a alternativa que indica todas as afirmativas corretas.
Provas
Provas
Provas
Identifique abaixo as afirmativas verdadeiras ( V ) e as falsas ( F ).
( ) O valor numérico da constante de equilíbrio de reações químicas sofre alteração quando há variação da temperatura da reação.
( ) A velocidade de reações químicas é alterada pela presença de catalisadores e estes (catalisadores) são totalmente consumidos durante a reação.
( ) A diminuição da temperatura de uma reação exotérmica desfavorece a formação de produtos.
( ) O tempo necessário para que a concentração do reagente se reduza a um quarto da concentração inicial é denominado de meia-vida.
( ) As leis de velocidades são determinadas experimentalmente e geralmente não podem ser escritas a partir da estequiometria da equação química da reação.
Assinale a alternativa que indica a sequência correta, de cima para baixo.
Provas
Provas
Provas
Provas
Provas
2. molaridade
3. fração molar
4. porcentagem massa/massa
( ) Quociente entre o número de mol do soluto e o número de mol total da solução.
( ) Quociente entre a massa do soluto em gramas e a massa da solução em gramas multiplicado por 100%.
( ) Relação do número de mols do soluto e a massa do solvente em quilogramas.
Provas
Caderno Container