Foram encontradas 150 questões.
Julgue o item a seguir, acerca de alguns aspectos da química de fármacos, produtos de limpeza e saponificação.
O fator polaridade é determinante na ação de sabões e detergentes, mas não tem importância significativa para o desenvolvimento de fármacos.
Provas
O modelo de obtenção de energia a partir da queima de combustíveis fósseis, adotado no início do desenvolvimento econômico industrial e cuja equação química geral é !$ \alpha !$CxH2x + 2 + !$ \beta !$O2 → !$ \gamma !$CO2 + !$ \eta !$H2O, tem apresentado várias conseqüências danosas para o atual estágio socioeconômico mundial. Uma delas é o aumento da concentração de óxidos no ar, tais como CO2, SO2, SO3, NO e NO2, que poluem a atmosfera. Esses óxidos reagem com a água da chuva, formando ácidos. Abaixo são representados alguns exemplos dessas reações.
I – CO2 + H2O → H2CO3
II – SO2 + ½ O2 + H2O → H2SO4
III – 2NO + O2 + H2O → HNO3 + HNO2
Os ácidos formados precipitam-se com a chuva, o que traz prejuízos para a agricultura, a vida aquática, a construção civil etc. Questões como essas, associadas à incerteza da quantidade de petróleo disponível no mundo, tornaram a pesquisa de outras fontes de energia uma prioridade na busca do bem-estar da humanidade e de um desenvolvimento economicamente sustentável. Diante dessa tarefa, a PETROBRAS já vem realizando pesquisas e decidiu que, até 2010, será uma companhia de energia e não mais uma empresa somente de petróleo e gás, o que justifica o seu slogan: DESAFIO, ESSA É A NOSSA ENERGIA!
Considerando o texto acima e sabendo que M(C) = 12 g/mol, M(O) = 16 g/mol e M(H) = 1 g/mol, julgue o item a seguir.
As substâncias elementares dos átomos representados nas equações I, II e III apresentam altas condutividades térmica e elétrica.
Provas
A chuva ácida é causada pela queima de combustíveis com alto conteúdo de enxofre. Para evitar esse sério problema ambiental, foram implementadas legislações para limitar o conteúdo máximo de enxofre (S) em combustíveis. Uma estratégia para diminuir o conteúdo dessa substância em combustíveis é oxidá-la, transformando-a em sulfóxidos menos voláteis ou sulfonas, que podem ser separadas mais facilmente do combustível. O conteúdo de enxofre em combustíveis pode ser determinado usando-se uma reação de combustão para converter enxofre em dióxido de enxofre. Este é coletado e borbulhado em uma solução aquosa de peróxido de hidrogênio (!$ H_2O_2 !$), produzindo-se ácido sulfúrico, que se pode titular com NaOH, o que provê uma determinação indireta de enxofre. As reações envolvidas nesse processo são representadas abaixo.
I !$ S(s) + O_2(g) \rightarrow SO_2(g) !$
II !$ SO_2(g) + H_2O_2(aq) \rightarrow H_2SO_4(aq) !$
III !$ H_2SO_4(aq) +2OH^(aq) \rightleftharpoons SO^{2-}_4(aq)+2H_2O(l) !$
Considerando que as constantes de dissociação ácida do ácido sulfúrico são !$ K_1 = \infty !$ e !$ K_2=1 \times 10^{-2} !$, que a constante de dissociação da água, !$ K_w !$, é igual a !$ 1 \times 10^{-14} !$ e que M(S) = 32 g/mol, julgue o item seguinte.
O ácido sulfúrico é considerado um ácido forte com relação ao 1.º hidrogênio dissociado.
Provas
Julgue o item a seguir, acerca de alguns aspectos da química de fármacos, produtos de limpeza e saponificação.
A produção de sabão é feita pela hidrólise alcalina de ésteres de ácidos graxos. Os sais obtidos são de difícil biodegradação, o que tem sido alvo de muitos estudos, devido aos problemas causados ao meio ambiente.
Provas
Provas
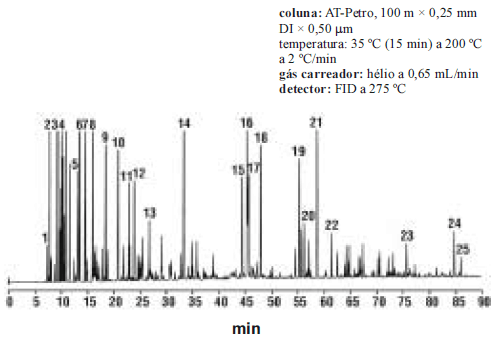
A chuva ácida é causada pela queima de combustíveis com alto conteúdo de enxofre. Para evitar esse sério problema ambiental, foram implementadas legislações para limitar o conteúdo máximo de enxofre (S) em combustíveis. Uma estratégia para diminuir o conteúdo dessa substância em combustíveis é oxidá-la, transformando-a em sulfóxidos menos voláteis ou sulfonas, que podem ser separadas mais facilmente do combustível. O conteúdo de enxofre em combustíveis pode ser determinado usando-se uma reação de combustão para converter enxofre em dióxido de enxofre. Este é coletado e borbulhado em uma solução aquosa de peróxido de hidrogênio (!$ H_2O_2 !$), produzindo-se ácido sulfúrico, que se pode titular com NaOH, o que provê uma determinação indireta de enxofre. As reações envolvidas nesse processo são representadas abaixo.
I !$ S(s) + O_2(g) \rightarrow SO_2(g) !$
II !$ SO_2(g) + H_2O_2(aq) \rightarrow H_2SO_4(aq) !$
III !$ H_2SO_4(aq) +2OH^(aq) \rightleftharpoons SO^{2-}_4(aq)+2H_2O(l) !$
Considerando que as constantes de dissociação ácida do ácido sulfúrico são !$ K_1 = \infty !$ e !$ K_2=1 \times 10^{-2} !$, que a constante de dissociação da água, !$ K_w !$, é igual a !$ 1 \times 10^{-14} !$ e que M(S) = 32 g/mol, julgue o item seguinte.
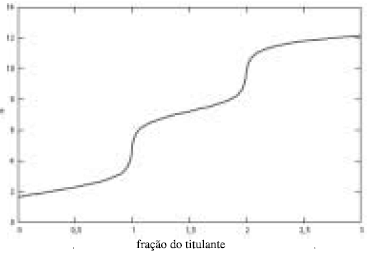
A curva de titulação do H2SO4 pelo NaOH pode ser corretamente representada pela figura abaixo.
Provas
No que se refere à Microbiologia, julgue o item que se segue.
A insulina produzida por uma bactéria, ainda que geneticamente modificada, não serve ao ser humano, pois as proteínas bacterianas são estruturalmente diferentes das humanas.
Provas
O modelo de obtenção de energia a partir da queima de combustíveis fósseis, adotado no início do desenvolvimento econômico industrial e cuja equação química geral é !$ \alpha !$CxH2x + 2 + !$ \beta !$O2 → !$ \gamma !$CO2 + !$ \eta !$H2O, tem apresentado várias conseqüências danosas para o atual estágio socioeconômico mundial. Uma delas é o aumento da concentração de óxidos no ar, tais como CO2, SO2, SO3, NO e NO2, que poluem a atmosfera. Esses óxidos reagem com a água da chuva, formando ácidos. Abaixo são representados alguns exemplos dessas reações.
I – CO2 + H2O → H2CO3
II – SO2 + ½ O2 + H2O → H2SO4
III – 2NO + O2 + H2O → HNO3 + HNO2
Os ácidos formados precipitam-se com a chuva, o que traz prejuízos para a agricultura, a vida aquática, a construção civil etc. Questões como essas, associadas à incerteza da quantidade de petróleo disponível no mundo, tornaram a pesquisa de outras fontes de energia uma prioridade na busca do bem-estar da humanidade e de um desenvolvimento economicamente sustentável. Diante dessa tarefa, a PETROBRAS já vem realizando pesquisas e decidiu que, até 2010, será uma companhia de energia e não mais uma empresa somente de petróleo e gás, o que justifica o seu slogan: DESAFIO, ESSA É A NOSSA ENERGIA!
Considerando o texto acima e sabendo que M(C) = 12 g/mol, M(O) = 16 g/mol e M(H) = 1 g/mol, julgue o item a seguir.
A neutralização de um ácido por uma base forma água e um sal, este formado pelo cátion da base e pelo ânion do ácido.
Provas
Julgue o item subseqüente, que se referem aos equipamentos comumente utilizados em um laboratório de Química.
Toda amostra ou substância química usada para fins analíticos deve ser pesada em balança analítica, sob pena de se comprometer a análise.
Provas
A chuva ácida é causada pela queima de combustíveis com alto conteúdo de enxofre. Para evitar esse sério problema ambiental, foram implementadas legislações para limitar o conteúdo máximo de enxofre (S) em combustíveis. Uma estratégia para diminuir o conteúdo dessa substância em combustíveis é oxidá-la, transformando-a em sulfóxidos menos voláteis ou sulfonas, que podem ser separadas mais facilmente do combustível. O conteúdo de enxofre em combustíveis pode ser determinado usando-se uma reação de combustão para converter enxofre em dióxido de enxofre. Este é coletado e borbulhado em uma solução aquosa de peróxido de hidrogênio (!$ H_2O_2 !$), produzindo-se ácido sulfúrico, que se pode titular com NaOH, o que provê uma determinação indireta de enxofre. As reações envolvidas nesse processo são representadas abaixo.
I !$ S(s) + O_2(g) \rightarrow SO_2(g) !$
II !$ SO_2(g) + H_2O_2(aq) \rightarrow H_2SO_4(aq) !$
III !$ H_2SO_4(aq) +2OH^(aq) \rightleftharpoons SO^{2-}_4(aq)+2H_2O(l) !$
Considerando que as constantes de dissociação ácida do ácido sulfúrico são !$ K_1 = \infty !$ e !$ K_2=1 \times 10^{-2} !$, que a constante de dissociação da água, !$ K_w !$, é igual a !$ 1 \times 10^{-14} !$ e que M(S) = 32 g/mol, julgue o item seguinte.
Durante a titulação, a adição de NaOH da bureta desloca o equilíbrio representado pela equação III, que ocorre no erlenmeyer, para a direita.
Provas
Caderno Container