Foram encontradas 2.827 questões.

Provas
Provas
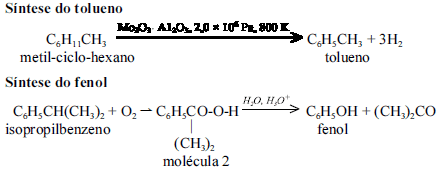
Provas
Provas
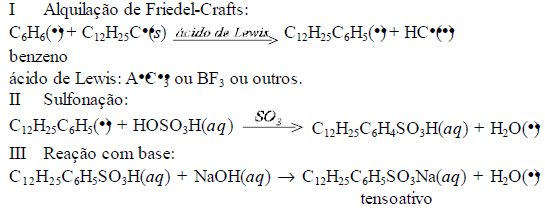
Provas
Provas
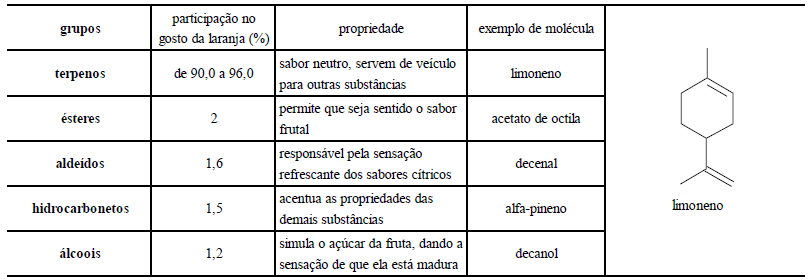
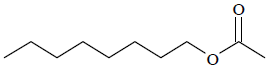
É quase impossível imaginar o mundo moderno sem o petróleo e seus subprodutos. A indústria petroquímica sintetiza, a partir de matérias-primas obtidas diretamente das refinarias, os produtos que terão aplicação em praticamente qualquer ramo industrial moderno. Um dos principais produtos sintetizados é o benzeno, largamente empregado como insumo em diversas fábricas. As indústrias de detergentes utilizam o benzeno na síntese do para-dodecil-benzeno-sulfonato de sódio, um dos tensoativos mais utilizados em detergentes e sabões em pó. As etapas da produção desse tensoativo são apresentadas a seguir.
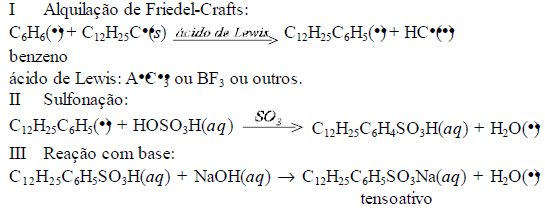
Sabendo que M(H) = 1 g/mol, M(C) = 12 g/mol e M(CR) = 35,5 g/mol, e considerando as informações acima, julgue o item que se segue.
Os coeficientes estequiométricos da equação química da etapa I indicam que a reação completa de 1 g de benzeno consome 1 g de C12H25C•.
Provas
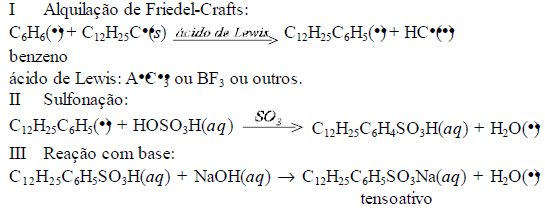
Provas
Provas


Provas
Caderno Container