Foram encontradas 60 questões.
- FundamentosPropriedades das Substâncias
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Transformações Químicas e EnergiaEletroquímica
l2 + Na2 S2 O3 → Nal + Na2 S4 O6
Na reação de oxirredução representada pela equação não balanceada acima, o número de oxidação médio do.
Na reação de oxirredução representada pela equação não balanceada acima, o número de oxidação médio do.
Provas
Questão presente nas seguintes provas
Utilize as informações contidas na Tabela de potenciais de redução abaixo para responder a questão.
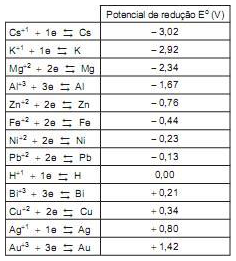
Dentre as opções abaixo, o metal que se oxida mais facilmente nas mesmas condições ambientais, frente a um mesmo oxidante, é o
Provas
Questão presente nas seguintes provas
Cinco cubos de gelo de 10 g, a temperatura de -5 °C, são adicionados à água a temperatura inicial de 70 °C. Após algum tempo, todos os cubos de gelo derretem integralmente.
A energia necessária para levar o gelo até a temperatura de fusão e a energia necessária para fundir o gelo, são, em J, respectivamente,
Considere
cgelo = 2,2 J/g K
LF =330 J/g
A energia necessária para levar o gelo até a temperatura de fusão e a energia necessária para fundir o gelo, são, em J, respectivamente,
Considere
cgelo = 2,2 J/g K
LF =330 J/g
Provas
Questão presente nas seguintes provas
Uma carreta transportando ácido sulfúrico concentrado tombou numa estrada. Parte do ácido vazou no asfalto.
Com o exclusivo objetivo de neutralizar o ácido, o procedimento correto deve ser o de jogar no asfalto solução aquosa de
Com o exclusivo objetivo de neutralizar o ácido, o procedimento correto deve ser o de jogar no asfalto solução aquosa de
Provas
Questão presente nas seguintes provas
Através de um processo de pirólise, o H2 se oxida para formar H2O de acordo com o processo descrito pela equação .
H2 + 1/2 O2 → H2O
Nesse processo, quantos mols de O2 são necessários para produzir 10 mols de H2 O?
H2 + 1/2 O2 → H2O
Nesse processo, quantos mols de O2 são necessários para produzir 10 mols de H2 O?
Provas
Questão presente nas seguintes provas
Utilize as informações contidas na Tabela de potenciais de redução abaixo para responder a questão.

Considere a pilha abaixo representada pela seguinte equação:![]()
Provas
Questão presente nas seguintes provas
Os hidrocarbonetos podem ser classificados de acordo com a proporção de átomos de carbono e hidrogênio presentes em sua composição química.
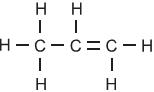
O hidrocarboneto apresentado na Figura acima é classificado como
Provas
Questão presente nas seguintes provas
Os eletrodos revestidos podem ser utilizados para a soldagem de aços-carbono. Nesse caso, eles são constituídos principalmente de uma alma metálica de aço de baixo carbono e do revestimento. Considere as afirmativas referentes às funções desse revestimento.
I - É função do revestimento impedir a mistura do material da alma metálica com o metal de solda.
II - É função do revestimento a remoção dos elementos de liga do metal de solda.
III - É função do revestimento o isolamento mecânico da alma metálica.
É correto APENAS o que se afirma em
I - É função do revestimento impedir a mistura do material da alma metálica com o metal de solda.
II - É função do revestimento a remoção dos elementos de liga do metal de solda.
III - É função do revestimento o isolamento mecânico da alma metálica.
É correto APENAS o que se afirma em
Provas
Questão presente nas seguintes provas
Uma massa de água m = 100 g está a uma temperatura inicial Ti = 30 o C. Essa massa é colocada em um refrigerador de modo que toda ela congela. Qual é, em J, a energia retirada para congelar os 100 g de água?
Qual é, em J, a energia retirada para congelar os 100 g de água?
Dados
Lfusão = 336 J/g
cágua = 4,2 J/g.° C
Qual é, em J, a energia retirada para congelar os 100 g de água?
Dados
Lfusão = 336 J/g
cágua = 4,2 J/g.° C
Provas
Questão presente nas seguintes provas
Uma típica reação química de hidratação de silicatos, que ocorre naturalmente com a mistura de cimento Portland e água, é dada por
2 Ca3 Si O5 + X H2O → ( 3 CaO . 2 Si O2 . 4 H2 O ) + Y Ca( OH)2 + 173,6 kJ
Os coeficientes estequiométricos X e Y são, respectivamente,
2 Ca3 Si O5 + X H2O → ( 3 CaO . 2 Si O2 . 4 H2 O ) + Y Ca( OH)2 + 173,6 kJ
Os coeficientes estequiométricos X e Y são, respectivamente,
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container