Foram encontradas 40 questões.
Um resistor ôhmico é submetido a uma diferença de potencial
de 220 V e uma intensidade de corrente elétrica
de 5,00 A.
A resistência elétrica desse resistor, em Ω, é igual a
A resistência elétrica desse resistor, em Ω, é igual a
Provas
Questão presente nas seguintes provas
- EletromagnetismoElétricaEletricidade
- EletromagnetismoElétricaForça Elétrica, Campo Elétrico e Eletrização
Quando colocada em um determinado ponto de um campo
elétrico, uma carga puntiforme de 2 x 10-3
C é submetida
a uma força de intensidade de 4 x 10-2
N.
A intensidade do campo elétrico, em N/C, é igual a
A intensidade do campo elétrico, em N/C, é igual a
Provas
Questão presente nas seguintes provas
Um recipiente de vidro tem seu volume de 500 cm3
completamente
preenchido por glicerina líquida a 30 °C. Esse
sistema é aquecido até a temperatura de 130 °C, quando
ocorre o transbordamento de 10 cm3
de glicerina. A variação de volume da glicerina com o aquecimento, em cm3
,
é igual a
Dado Coeficiente de dilatação volumétrica do vidro: 3,0 x 10-4 °C-1
Dado Coeficiente de dilatação volumétrica do vidro: 3,0 x 10-4 °C-1
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
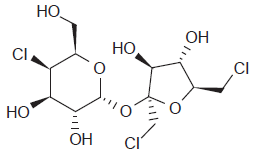
A sucralose é um edulcorante amplamente consumido.
Provas
Questão presente nas seguintes provas
A liberação de calor proveniente da combustão da glicose
(C6
H12O6
) é de 2.600 kJ de energia por cada 1 mol. Um
atleta olímpico precisa de 10.140 kJ por dia, quando em
treinamento prévio a uma grande competição.
Ao expressar essa energia em termos de massa de glicose, o atleta deve ingerir, em gramas, aproximadamente,
Dado M(C) = 12 g mol-1 M (O) = 16 g mol-1 M(H) = 1 g mol-1
Ao expressar essa energia em termos de massa de glicose, o atleta deve ingerir, em gramas, aproximadamente,
Dado M(C) = 12 g mol-1 M (O) = 16 g mol-1 M(H) = 1 g mol-1
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasPropriedades Coligativas: Tonoscopia, Ebulioscopia, Crioscopia e Pressão Osmótica.
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Uma solução para remoção de esmalte foi preparada,
misturando-se 176,0 g de acetato de etila e 29,0 g de acetona.
Considerando-se a temperatura de 20 ºC, a razão entre a pressão de vapor da acetona pura e a pressão de vapor do removedor de esmalte é, aproximadamente,
Dado Pressão de vapor do acetato de etila: 73 mmHg a 20 ºC Pressão de vapor da acetona: 200 mmHg a 20 ºC M (acetato de etila) = 88,0 g mol-1 M (acetona) = 58,0 g mol-1
Considerando-se a temperatura de 20 ºC, a razão entre a pressão de vapor da acetona pura e a pressão de vapor do removedor de esmalte é, aproximadamente,
Dado Pressão de vapor do acetato de etila: 73 mmHg a 20 ºC Pressão de vapor da acetona: 200 mmHg a 20 ºC M (acetato de etila) = 88,0 g mol-1 M (acetona) = 58,0 g mol-1
Provas
Questão presente nas seguintes provas
A reação de oxirredução que ocorre numa pilha de lítio é representada simplificadamente a seguir:
2 Li(s) + I2(s) → 2 Li+ (aq) + 2 I- (aq)
Dados os potenciais padrões de redução:
• Eº Li+ /Li = -3,05 V
• Eº I2 /I- = +0,53 V
verifica-se que a diferença de potencial padrão dessa pilha, em volts, é
Provas
Questão presente nas seguintes provas
Uma solução líquida contém duas substâncias denominadas
I e II. Um volume de 100 microlitros da solução foi
colocado perto da borda inferior (na linha da amostragem)
de uma placa de cromatografia de camada delgada, cuja
fase estácionária tem caráter mais polar. A borda inferior
da placa foi mergulhada em solvente de caráter menos
polar, de forma que este, por capilaridade, percolasse a
fase estacionária. Após 5 minutos, a linha de frente foi
marcada 10,0 cm acima da linha de amostragem.
Sabendo-se que o fator de retenção (RF) da substância I foi de 0,9, que o da substância II foi de 0,6 e que os diâmetros das manchas foram de 0,2 cm, conclui-se que a
Sabendo-se que o fator de retenção (RF) da substância I foi de 0,9, que o da substância II foi de 0,6 e que os diâmetros das manchas foram de 0,2 cm, conclui-se que a
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
- Transformações Químicas e EnergiaEletroquímica
A medição de pH de uma solução aquosa é feita usando-se o eletrodo combinado de membrana de vidro.
Nessa medição, há eletrodo de
Nessa medição, há eletrodo de
Provas
Questão presente nas seguintes provas
Uma mistura gasosa contém H2
e Ne, exercendo pressão
total de 5 atm, sob condições ideais.
Sabendo-se que a massa de Ne na mistura é 4 vezes maior que a massa de H2 , a pressão parcial do H2 , em atm, teria um valor mais próximo de
Dado M (H2 ) = 2 g mol-1 M (Ne) = 20 g mol-1 (RT/V) = 1 atm mol-1
Sabendo-se que a massa de Ne na mistura é 4 vezes maior que a massa de H2 , a pressão parcial do H2 , em atm, teria um valor mais próximo de
Dado M (H2 ) = 2 g mol-1 M (Ne) = 20 g mol-1 (RT/V) = 1 atm mol-1
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container