Foram encontradas 60 questões.
Para a preparação de soluções no dia a dia, um laboratorista deve fazer uso de:
Provas
Analise as assertivas abaixo sobre conduta e segurança no laboratório de química:
I. Os cabelos compridos devem ser mantidos sempre presos para evitar que se prendam a materiais ou equipamentos ou até mesmo que sejam atingidos por produtos químicos ou fogo.
II. Todos os produtos químicos devem estar devidamente rotulados.
III. É indispensável o uso de avental longo, em tecido de algodão, sobre a roupa.
IV. Sempre que necessário, dependendo do risco e da periculosidade, o experimento ou parte dele deverá ser conduzido em capela, utilizando-se EPIs como luvas, máscaras e óculos de proteção.
Quais estão corretas?
Provas
Relacione a Coluna 1 à Coluna 2, com base no tipo de luva descrito e sua respectiva utilização.
Coluna 1
1. Luvas nitrílicas.
2. Luvas de proteção térmica.
3. Luvas de látex para procedimentos.
4. Luvas de látex natural (amarelas).
Coluna 2
( ) No manuseio de materiais aquecidos ou resfriados, como estufas, autoclaves, fornos e ultrafreezers. Tipo: luvas de fio de kevlar tricotado. Protegem em trabalhos a temperaturas até 25ºC.
( ) Na lavagem de materiais e vidrarias. Protegem contra produtos químicos e umidade. Por serem mais espessas, promovem maior proteção contra cortes.
( ) No manuseio de amostras e em procedimentos com material biológico, sem a presença de produtos químicos.
( ) No manuseio de amostras e em procedimentos com produtos químicos, inclusive no preparo de soluções.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Provas
Um laboratorista precisa separar dois peptídeos. Sabe-se que o peptídeo A possui uma carga final de -2, enquanto o peptídeo B tem carga final de +1. Sobre isso, analise as assertivas abaixo:
I. A análise gravimétrica é a mais indicada para separação de peptídeos.
II. Com o auxílio de uma resina de troca iônica, é possível separar o peptídeo A e o peptídeo B, pois um dos peptídeos irá interagir mais fortemente do que o outro, logo ficará mais tempo retido, enquanto o outro elui.
III. Peptídeos com carga positiva têm mais facilidade em eluir do que peptídeos negativos quando analisados por cromatografia gasosa por captura de elétrons.
Quais estão INCORRETAS?
Provas
Analise o trecho e a imagem a seguir:
, em geral, possuem em sua estrutura: um grupo carboxílico (COOH) de caráter , um grupo amino (NH2) de caráter , um grupo orgânico (R) e um hidrogênio ligados em um carbono assimétrico (carbono α), conforme a figura abaixo. Assim, por apresentarem simultaneamente caracteres ácidos e básicos, são denominados compostos e são capazes de reagir com ácidos e bases.
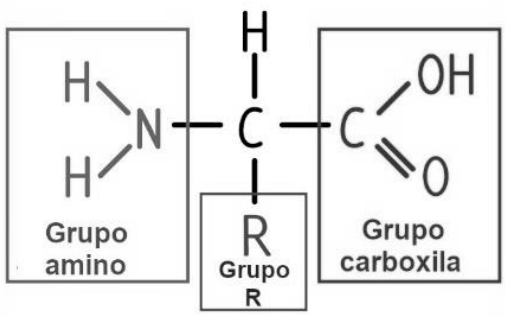
Assinale a alternativa que preenche, correta e respectivamente, as lacunas do trecho acima.
Provas
Determine a porcentagem de água e a fórmula molecular do cloreto de ferro hidratado (FeC!$ ℓ !$x∙yH2O). Considere para os cálculos massa molecular 270,5, com 20,6% de ferro e 39,4% de cloro, em massa.
Provas
Observe a equação abaixo e analise as assertivas a seguir, assinalando V, se verdadeiras, ou F, se falsas.
CO (g)+ 2 H2 (g) !$ \rightleftharpoons !$ H3COH (g) ΔH < 0
( ) A adição de um catalisador não desloca o equilíbrio da reação.
( ) A diminuição da temperatura irá deslocar o equilíbrio para a esquerda.
( ) Um aumento na concentração de monóxido de carbono irá deslocar a reação para a direita.
( ) Quando ocorre um aumento de pressão, o equilíbrio desloca-se para o lado de menor volume, ou seja, o lado que possuiu o menor número de mol.
( ) Ao diminuir a concentração de H3CO, ocorre o deslocamento do equilíbrio para a esquerda, favorecendo a formação de H2.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Provas
Calcule o valor da constante de equilíbrio Kc (em termo de concentração) para a reação a seguir, na temperatura de 400°C. Considere a constante de equilíbrio em temos de pressão (Kp), para a mesma reação, igual a 3,1∙10-4. Dados: R = 8,314 L∙kPa∙K-1 ∙mol-1.
2 SO2 (g)+ O2 (g) !$ \rightleftharpoons !$ 2 SO3 (g)
Provas
O álcool etílico, também chamado de etanol, é o álcool presente nas bebidas alcoólicas. Considere para cada copo de 120 mL de uma determinada marca de cachaça a presença de 45,8 mL de álcool etílico e determine a graduação alcoólica dessa bebida, calculando a porcentagem em volume.
Provas
Observe as moléculas a seguir e analise as assertivas abaixo:
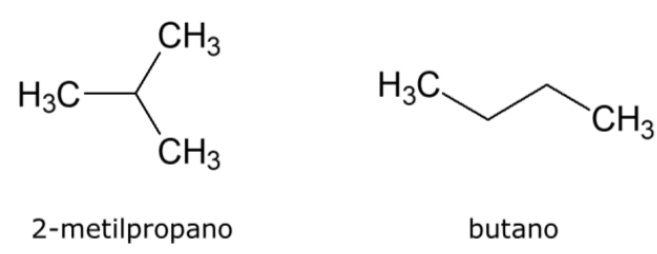
I. O butano apresenta ponto de ebulição mais elevado do que o 2-metilpropano.
II. O 2-metilpropano e o butano são hidrocarbonetos com fórmula molecular C4H10.
III. O 2-metilpropano é uma molécula polar enquanto o butano é uma molécula apolar.
Quais estão corretas?
Provas
Caderno Container