Foram encontradas 50 questões.
A reação à seguir descreve a síntese da amônia, conhecida por síntese de Haber- Bosh: N2(g) + 3H2(g) → 2NH3(g) . Se esse processo for realizado nas condições normais de temperatura e pressão, o volume de amônia produzido na reação total de 300 gramas de gás hidrogênio (H2(g)) será de Dados: Massa Molar H2(g) = 2g/mol.
Volume molar de gás nas CNTP = 22,4L/mol.
Provas
Um técnico preparou 500 mL de solução de sulfato de cobre II de concentração molar 0,250M. Para poder usar a mesma solução em um procedimento analítico, esse técnico precisou diluir a solução até a concentração de 15,95g/L. O volume final da solução diluída que ele vai obter após o procedimento é de Dados: massas atômicas:
Cu = 63,5u; S = 32u; O = 16u.
Provas
Assinale a alternativa que NÃO apresenta um dos deveres do técnico responsável pela lavagem das vidrarias.
Provas
Para um processo de avaliação experimental, um técnico deve escrever 4 rótulos contendo, separadamente, as fórmulas dos seguintes reagentes: 1 - Nitrato de ferro II, 2 - nitrato de prata, 3 - cloreto de potássio e 4 - carbonato de sódio. Assinale a alternativa que rotula, respectivamente, os frascos de 1 a 4
Provas
Na análise volumétrica de 0,960g de uma amostra de ácido cítrico, foram gastos 30mL de uma solução de NaOH 0,100 mol/L. Considerando que a reação NÃO balanceada entre o ácido cítrico e o hidróxido de sódio seja:
C6H8O7 + NaOH → C6H5O7Na3 + H20
Dessa forma, a pureza da amostra de ácido cítrico é de
Dados: Massa molar do ácido cítrico é igual a 192g/mol.

Provas
O eugenol (C 10H 12O 2), essência extraída do cravo-da-índia e usado como antisséptico bucal, apresenta em sua fórmula estrutural, representada pela figura a seguir, as seguintes funções orgânicas:
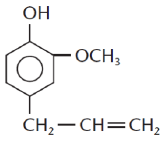
Provas
Dada a reação:
2 NH4NO3(s) → 2 N2(g) + O2(g) + 4 H2O(l) ΔH = - 411,2 kJ
A massa de nitrato de amônio com 80% de pureza necessária para a liberação de 0,979kcal de energia é igual a
Dados: Massa Molar NH4NO3 = 80g/mol; 1 cal é aproximadamente 4,2J.
Provas
Para o preparo de 5 litros de uma solução de sacarose 0,02M (C12H22O11 342g/mol), deve-se aferir, em uma balança analítica, uma massa de
Provas
Dizemos que uma solução está tamponada quando ela “resiste” às variações de pH. Nos laboratórios, as soluções-tampão são, em geral, uma solução de um ácido fraco e um sal correspondente a esse ácido ou uma solução de uma base fraca e um sal correspondente a essa base. Dessa forma, assinale a alternativa que NÃO corresponda a uma solução-tampão
Provas
Uma das técnicas mais utilizadas no dia a dia do laboratório de química é a diluição de soluções, que é o processo de adicionar à solução o próprio solvente para torná-la menos concentrada. Determine o volume de solvente que deve ser adicionado a 1000 mL de uma solução aquosa de NaOH de concentração 2 mols/L para que sua concentração final seja igual a 0,8 g/L.
Dados: massas atômicas:
Na = 23u; O = 16u, H = 1u.
Provas
Caderno Container