Foram encontradas 40 questões.
Quando vapores de ácido clorídrico e amônia aquosa entram em contato, ocorre a seguinte reação espontânea, produzindo uma “nuvem branca” de NH4Cl:
!$ HCl_{(g)} \, + \, NH_{3(g)} \, \rightarrow \, NH_4Cl_{(s)} !$
Definindo este como o sistema em estudo, se prevê que os sinais de !$ \Delta S^o, \, \Delta H^o, \, \Delta G^o, !$ são, respectivamente,
Provas
Questão presente nas seguintes provas
Considere as seguintes equações termoquímicas:
I. AlCl3 + Cl- !$ \rightarrow !$ [AlCl4]-
II. H3N + AlCl3 !$ \rightarrow !$ [H3N – AlCl3]
III. AlCl3 + CH3COCl !$ \rightarrow !$ [AlCl4]-[CH3CO]+
Segundo os critérios de Lewis, a substância AlCl3 é classificada como
Provas
Questão presente nas seguintes provas
Muitos gases colaboram na acidez das chuvas, dentre eles estão aqueles oriundos da decomposição do ácido carbônico e do ácido sulfuroso.
Ácido carbônico !$ \rightarrow !$ gás X + ...
Ácido sulfuroso !$ \rightarrow !$ gás Y + ...
Quanto à geometria e à polaridade das moléculas desses gases, é correto afirmar que:
Provas
Questão presente nas seguintes provas
A hemoglobina tem um papel importante em uma série de equilíbrios, envolvendo protonação-desprotonação e oxigenação-desoxigenação. A reação total é, aproximadamente, como segue:
Sobre o equilíbrio químico, envolvendo a hemoglobina considere os itens a seguir:
I. A concentração de O2 é maior nos pulmões e menor nos tecidos. Assim, uma alta [O2] desloca o equilíbrio para a direita, provocando um ligeiro aumento na acidez.
II. O pH normal plasmático é 7,4. Se o pH do sangue é reduzido pela presença de grandes quantidades de produtos ácidos do metabolismo, uma condição conhecida como acidose acontece. Com o quadro de acidose estabelecido, a capacidade da hemoglobina de transportar oxigênio diminui.
III. Na disfunção conhecida como alcalose metabólica, a capacidade da hemoglobina de transportar oxigênio diminui, o que dificulta a manutenção do pH plasmático.
Está(ão) correta(s) a(s) afirmativa(s):
Provas
Questão presente nas seguintes provas
A célula galvânica: !$ Cr_{(s)} \mid \, Cr^{+3} \, (aq., \, 0,10 \, mol) \mid \mid Pb^{+2}(aq., \, 1,00 \, \times \, 10^-2 mol/L) \mid \, Pb_{s} !$, apresenta como cátodo ______________, gera uma diferença de potencial no valor de ______________ sendo um processo _______________.
Sabendo que:
Cr(s) !$ \rightarrow !$ Cr+3(aq.) + 3e-
Pb(s) !$ \rightarrow !$ Pb+2(aq.) + 2e-
Eº= + 0,74V
Eº= + 0,126V
A alternativa que preenche, corretamente as lacunas, é:
Provas
Questão presente nas seguintes provas
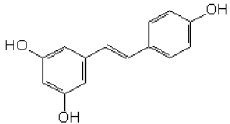
O etenilbenzeno ou fenileteno é conhecido como estireno, e o m-diidróxibenzeno é conhecido como resorcinol. A partir dessas informações, pode atribuir-se ao resveratrol, representado abaixo, o seguinte nome:
Provas
Questão presente nas seguintes provas
Com base no seguinte perfil de reação, indique a alternativa que completa as questões:
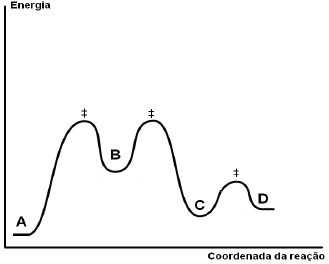
I. Quantos intermediários participam na reação A !$ \rightarrow !$ D?
II. Quantos Complexos Ativados existem?
III. Qual é a etapa mais rápida?
IV. A reação A !$ \rightarrow !$ D é exotérmica ou endotérmica?
Provas
Questão presente nas seguintes provas
Considere os seguintes compostos:
I. hidróxi-benzeno
II. etanol
III. propanona
IV. ácido etanóico
A ordem crescente correta de acidez é
Provas
Questão presente nas seguintes provas
Na presença de condições reacionais adequadas, o benzeno sofre reação de substituição eletrofílica aromática com uma grande variedade de reativos orgânicos ou inorgânicos. Por exemplo, na presença de água de bromo e tricloreto de alumínio, observa-se a seguinte reação:
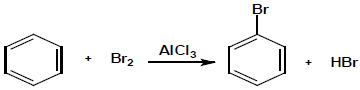
Grupos ligados ao anel benzênico interferem em sua reatividade. Alguns grupos tornam as posições orto e para mais suscetíveis de reações de substituição, enquanto outros grupos tornam a posição meta mais reativa.
Considerando o mecanismo dessa ativação e a natureza dirigente dos grupos presentes no anel, o principal produto da reação do 4-nitrofenol com bromo, na presença do catalisador AlCl3, é
Provas
Questão presente nas seguintes provas
Nenhum dos elementos do grupo 13 reage diretamente com o hidrogênio, mas diversos hidretos interessantes são conhecidos. Os hidretos de boro são também denominados boranos, por analogia com os alcanos (hidrocarbonetos). O diborano é o mais simples desses hidretos, é empregado na obtenção de boranos superiores e constitui um reagente importante na síntese orgânica.
Utilizando as seguintes informações termoquímicas, calcule a entalpia padrão de formação do diborano gasoso.
4 B (s) + 3 O2 (g) !$ \rightarrow !$ 2 B2O3 (s); !$ \Delta !$H0 = -2509,1 kJ.
2 H2 (g) + O2 (g) !$ \rightarrow !$ 2 H2O (l); !$ \Delta !$H0 = -571,7 kJ.
B2H6 (g) + 3O2 (g) !$ \rightarrow !$ B2O3 (s) + 3 H2O; !$ \DElta !$H0 = -2147,5 kJ.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container