Foram encontradas 50 questões.
As estruturas de Lewis 1, 2 e 3 estão representadas com todas as ligações e os pares de elétrons não ligantes, entretanto, as cargas formais, caso existam, não estão explicitadas.
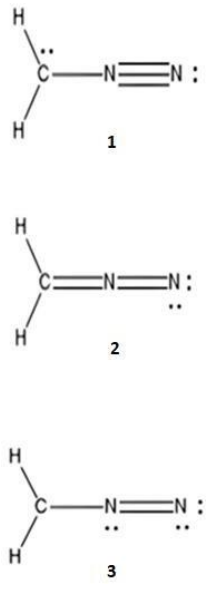
Dadas as afirmativas relativas às estruturas 1, 2 e 3,
I. 1, 2 e 3 são isômeros constitucionais.
II. 1, 2 e 3 são contribuintes de ressonância.
III. A estrutura 3 tem um carbono com carga positiva.
IV. A estrutura 1 tem um nitrogênio com carga negativa.
verifica-se que estão corretas
Provas
Uma empresa de engenharia submarina investiga a durabilidade de um trecho de duto de aço carbono exposto à água do mar. No ambiente marinho, a superfície de aço está sujeita, simultaneamente, à reação anódica de dissolução do ferro (Fe → Fe2+ + 2 e−) e à reação catódica de redução de oxigênio dissolvido (O2 + 4 H+ + 4 e− → 2 H2O, em meios ácidos, ou O2 + 2 H2O + 4 e− → 4 OH−, em meio neutro/ácido físico).
Para descrever a taxa de corrosão do aço, o grupo utiliza a teoria do potencial misto (mixed potential theory), medindo o potencial de corrosão (Ecor) em circuito aberto e a densidade de corrente de corrosão (icor) a partir das curvas de polarização anódica e catódica.
Considerando, exclusivamente, esses conceitos de eletroquímica, assinale a alternativa correta.
Provas
Uma indústria de tratamento de superfícies metálicas utiliza um processo eletroquímico para proteger peças de aço contra corrosão por meio de deposição de cobre metálico. O processo ocorre em uma célula eletrolítica, contendo solução aquosa de CuSO4 0,50 mol/L. A peça de aço funciona como cátodo, enquanto um eletrodo inerte de platina é utilizado como ânodo.
Durante a operação, uma corrente elétrica constante de 4,82 A é aplicada por 40 minutos. Considere:
- constante de Faraday (F) = 96.500 C/mol
- massa molar do cobre (Cu) = 63,5 g/mol
- reação que ocorre no cátodo: Cu\( _{\left(aq\right)}^{2+} \) + 2 e− → Cu(s)
Despreze reações paralelas e considere eficiência de corrente igual a 100%.
Com base nessas informações, qual é a massa aproximada de cobre depositada sobre a peça metálica ao fim do processo?
Provas
Considere a reação, em fase gasosa, que ocorre a volume constante de 1,00 L.
A(g) + 2B(g) ; C(g) + D(g)
No início, o sistema contém apenas 2,00 mols de A e 4,00 mols de B. Para esta reação, a 298 K, a constante de equilíbrio vale Kc = 0,25 L. mol−1.
Assinale a alternativa que apresenta o valor correto da extensão da reação ( (em mol) no equilíbrio.
Provas
Em um recipiente fechado e rígido de volume V, mantido a uma temperatura constante T, estabelece-se o equilíbrio heterogêneo da reação de decomposição do carbamato de amônio.
2 NH2COONH4(s) ; 2NH3(g) + CO2(g)
Considere que o sólido presente é puro, que os gases se comportam idealmente e que o sistema foi iniciado apenas com o sólido, sem gases presentes. Após tempo suficiente, o sistema atinge o equilíbrio.
Dadas as afirmativas sobre três intervenções independentes, mantendo-se a temperatura constante e que contém sólido no recipiente após cada intervenção,
I. A adição de uma massa adicional de carbamato de amônio sólido ao recipiente, após o equilíbrio ter sido atingido, não provoca alteração nas pressões parciais de NH3 e CO2.
II. Se uma porção da mistura gasosa for rapidamente removida por uma válvula e o sistema for novamente isolado, o equilíbrio será deslocado para a direita. Ao atingir o novo equilíbrio, a pressão total no interior do recipiente retornará ao mesmo valor da pressão total medida antes da retirada dos gases.
III. A introdução do gás Hélio no sistema, aumentará a pressão total do sistema, mas não alterará o valor do quociente de reação (definido em termos de pressões parciais), mantendo-se o equilíbrio inalterado.
verifica-se que está/ão correta/s
Provas
Dadas as afirmativas sobre as propriedades termodinâmicas de espécies iônicas em solução,
I. Pela lei limite de Debye–Hückel, ao se aumentar a força iônica do meio, a blindagem eletrostática diminui, de modo que o alcance das interações coulombianas entre íons aumenta; além disso, os coeficientes de atividade afastam-se menos do ideal em soluções mais concentradas.
II. A equação de Born permite estimar a energia de Gibbs de solvatação de um íon, tratando-o como uma esfera carregada em um contínuo dielétrico; assim, a solvatação torna-se mais favorável (ΔG mais negativo) quanto maior o módulo da carga do íon e quanto maior a constante dielétrica do solvente, e torna-se menos favorável quanto maior o raio iônico efetivo.
III. A equação de Nernst relaciona o potencial de uma pilha à composição do sistema reacional, por meio de uma medida de “tendência” baseada em atividades; em soluções suficientemente diluídas, essas atividades podem ser aproximadas por concentrações, enquanto, em meios mais concentrados, essa aproximação falha e o potencial reflete os desvios de idealidade.
verifica-se que está/ão correta/s
Provas
Considere a reação \( A \) → B de terceira ordem. Se a constante de velocidade vale 0,15 L² . mol⁻² . s⁻¹, a concentração molar inicial da espécie A vale 1,00 mol L⁻¹.
Assinale a alternativa correta que indica o tempo, em segundos, necessário para que a concentração de A seja de 0,25 mol.L⁻¹.
Provas
Dadas as afirmativas sobre cinética química,
I. Pode-se obter a energia de ativação determinando-se o coeficiente linear da reta obtida no gráfico de Arrhenius (logaritmo da constante de velocidade em função do inverso da temperatura). Quanto mais inclinada for a reta no gráfico, mais forte será a dependência entre a constante de velocidade e a temperatura.
II. A ordem de uma reação é uma grandeza empírica, obtida da lei de velocidade levantada experimentalmente. Já a molecularidade de uma reação é a propriedade de uma reação elementar que faz parte de um mecanismo teórico de interpretação da reação.
III. No mecanismo de Lindemann-Hinshelwood, a velocidade da reação atinge um patamar constante de saturação, porque todos os sítios ativos das moléculas de gás estão ocupados pelo substrato, impedindo a formação do produto.
Verifica-se que está/ão correta/s
Provas
A meia vida é um parâmetro conveniente de uma reação química, pois trata-se do intervalo de tempo (t) necessário para a concentração de um reagente, [A], cair à metade do seu valor inicial.
Considere a reação \( A \) → \( P \), a qual segue a lei de uma cinética de segunda ordem, para o consumo do reagente A.
Assinale a alternativa que apresenta a correta expressão para o tempo de meia vida (\( t \)1/2), em função da concentração inicial do reagente A,[\( A \)]0, e da contante de velocidade (k) para a reação de segunda ordem considerada.
Provas
Dadas as afirmativas relacionadas à termoquímica e à termodinâmica química,
I. Quando um sistema se expande livremente, o trabalho é o maior possível, pois o sistema se expande no vácuo.
II. Em um sistema fechado, contendo um gás ideal, entre os mesmos estados inicial e final, mantido em contato com um reservatório térmico, o processo isotérmico reversível é o que produz o maior trabalho.
III. Em sistemas abertos operando em regime permanente, a variação de entalpia entre a entrada e a saída participa do balanço de energia, junto ao calor trocado, ao trabalho de eixo e à energia associada ao escoamento do fluido.
IV. A entalpia de uma reação química é invariável com a pressão para qualquer sistema, desde que a temperatura seja mantida constante e não ocorram mudanças de fase.
verifica-se que estão corretas apenas
Provas
Caderno Container