Foram encontradas 60 questões.
- Interações com Tecnologia, Sociedade e Meio Ambiente
- Química CinéticaRepresentação das Transformações Químicas
- Transformações Químicas e EnergiaTermoquímica
A Tabela abaixo indica alguns parâmetros da gasolina (representada por C8H18) e do etanol (C2H6O).
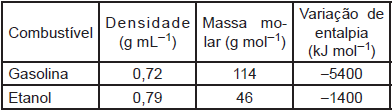
Comparando-se a combustão completa de 1,0 L de cada combustível, verifica-se que a razão entre o calor produzido pela gasolina e o produzido pelo etanol é:

Comparando-se a combustão completa de 1,0 L de cada combustível, verifica-se que a razão entre o calor produzido pela gasolina e o produzido pelo etanol é:
Provas
Questão presente nas seguintes provas
Considere os seguintes átomos dos elementos químicos (neutros ou ionizados) a seguir:
Tc Ru Pd2+ Ag+ Cd2+
Dentre esses átomos, possuem a mesma quantidade de elétrons o:
Tc Ru Pd2+ Ag+ Cd2+
Dentre esses átomos, possuem a mesma quantidade de elétrons o:
Provas
Questão presente nas seguintes provas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
A seguir, está representada uma substância química que possui atividade biológica.
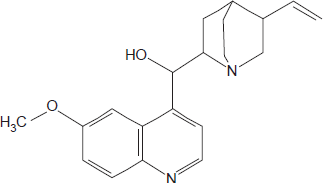
Nessa substância, estão presentes as funções orgânicas.

Nessa substância, estão presentes as funções orgânicas.
Provas
Questão presente nas seguintes provas
A Figura abaixo representa a estrutura de um composto que possui fórmula molecular C8H16O.
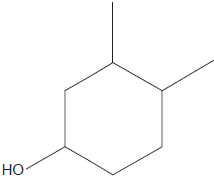
De acordo com as regras da IUPAC, o nome do composto é:

De acordo com as regras da IUPAC, o nome do composto é:
Provas
Questão presente nas seguintes provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
Sólidos incrustados nos dutos de prospecção de petróleo ocorrem por conta da formação de precipitados formados a partir dos íons presentes na água prospectada junto com o óleo. A precipitação é um processo exotérmico, e o valor de produto de solubilidade (a 25 ºC em água) para o sulfato de bário é 1 x 10-10 e para o sulfato de cálcio é 2 x 10-5.
Com base nas informações, tem-se que o(a)
Com base nas informações, tem-se que o(a)
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Químico na Água
Uma massa de 50,00 g de óleo foi dissolvida totalmente em uma mistura de água, isopropanol e tolueno. Essa solução foi titulada com uma solução alcoólica de hidróxido de potássio 0,10 mol L-1, e o ponto de equivalência foi atingido com 2,5 mL.
O índice de acidez do óleo, expresso em miligramas de KOH por cada 1(um) grama de óleo, é igual a:
Dado Massa molar do KOH = 56 g mol-1
O índice de acidez do óleo, expresso em miligramas de KOH por cada 1(um) grama de óleo, é igual a:
Dado Massa molar do KOH = 56 g mol-1
Provas
Questão presente nas seguintes provas
Com relação à presença de compostos nitrogenados no petróleo e em suas frações, sabe-se que.
Provas
Questão presente nas seguintes provas
Dos aparatos de medição de volume listados abaixo, o que mediria um volume contido de 10,00 mL com maior precisão é a(o).
Provas
Questão presente nas seguintes provas
Os potenciais padrões de redução de alguns sistemas encontram-se abaixo.
Ag+ + e → Ag(s); Eº = +0,80 V. Cu2+ + 2e → Cu(s); Eº = +0,34 V. Cd2+ + 2e → Cd(s); Eº = -0,40 V. Zn2+ + 2e → Zn(s); Eº = -0,76 V.
Levando-se em conta a espontaneidade dos processos,
Ag+ + e → Ag(s); Eº = +0,80 V. Cu2+ + 2e → Cu(s); Eº = +0,34 V. Cd2+ + 2e → Cd(s); Eº = -0,40 V. Zn2+ + 2e → Zn(s); Eº = -0,76 V.
Levando-se em conta a espontaneidade dos processos,
Provas
Questão presente nas seguintes provas
- Gases
- Química CinéticaRepresentação das Transformações Químicas
- Química CinéticaTransformações Químicas
Um volume de 5,0 L, medidos na CNTP, de uma amostra de gás natural foi queimado (combustão completa). Se a amostra tem composição, em volume, de 90% de metano e 10% de etano, o item que indica, com a melhor aproximação, a massa de CO2 produzida, em gramas, é:
Dados
CNTP: 1 atm e 273 K R = 0,082 atm L mol-1 K-1
CNTP: 1 atm e 273 K R = 0,082 atm L mol-1 K-1
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container