Foram encontradas 65 questões.
A determinação de H2S em um gás natural foi feita por titulação iodométrica através do seguinte procedimento: 100L de gás natural foram passados em uma torre de absorção contendo solução neutra de Cd+2, onde o H2S foi retido na forma de CdS. A mistura foi acidificada e tratada com 10,00mL de solução aquosa 0,0150mol/L de I3 −1, sendo o excesso de I3 −1 titulado com 20,00mL de solução 0,0100mol/L de S2O3−2, conforme as reações abaixo.
|
S−2 (aq) + I3 −1 (aq) → S(s) + 3I−1 (aq) I3 −1 (aq) + 2S2O3 −2 (aq) → 3I−1 (aq) + S4O6 −2 (aq) |
O teor de H2S no gás natural, em mg/m3, é de:
Provas
Os substratos abaixo reagem com HNO3 para a obtenção de produtos mononitrados. O substrato mais reativo para condições idênticas de reação é o:
Provas
Dentre os compostos a seguir, conhecidos por suas propriedades antidetonantes, qual apresenta a geometria de uma bipirâmide trigonal?
Provas
Avaliando o primeiro potencial de ionização dos elementos na tabela periódica, é correto afirmar que a tendência periódica desta propriedade é de crescer com o aumento do(a):
Provas
O composto abaixo é um produto excretado pelo organismo após a ingestão do fármaco diazepam, empregado no tratamento da ansiedade.
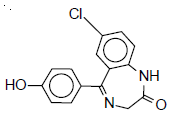
As funções orgânicas presentes na molécula deste composto são:
Provas
Em uma cuba eletrolítica adiciona-se uma solução 1mol/L de AgNO3. Nesta solução é imerso um bastão de zinco. Em outra cuba, adiciona-se uma solução 1mol/L de ZnSO4, onde é imerso um bastão de prata. Baseado nos valores dos potenciais-padrão de redução da prata e do zinco, assinale a opção que relaciona corretamente o sentido da reação e a diferença de potencial da pilha.
(Dados: E° Ag1+ / Ag° = 0,799V
E° Zn2+ / Zn°= − 0,763V)
Provas
Considere as estruturas químicas das aminas abaixo.
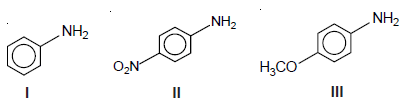
A ordem crescente de basicidade dessas aminas é:
Provas
A figura abaixo mostra um cromatograma obtido em condição de isoterma utilizando a cromatografia gasosa de alta resolução com detector de ionização por chama.
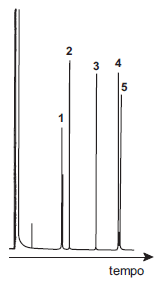
A resolução cromatográfica entre os picos 4 e 5 pode ser melhorada com a(o):
Provas
Sabendo-se que o calor de combustão do etino é −1301kJ/mol e o do etano é −1561kJ/mol, a 25 °C e 1atm, o calor de hidrogenação total, em kJ/mol, para o etino será:
(Dado: H2(g) + ½ O2 (g) !$ \longrightarrow !$ H2O (!$ \ell !$) !$ \Delta H !$ = −286kJ/mol)
Provas
O uso de brancos de titulação em análises titrimétricas é recomendado para estimar possíveis erros ocorridos durante o procedimento analítico. Na análise de brometo pelo Método Mohr, pesam-se cerca de 3,0000g de KBr, dissolve-se o sal em água e avoluma-se a solução em balão volumétrico de 250mL. Em seguida, pipetam-se 25mL desta solução, transferindo-a para um erlenmeyer de 250mL. Adicionam-se 75mL de água, 1mL de solução de ácido acético 6mol/L e 10 gotas de solução hidroalcoólica de eosina. A titulação é efetuada com solução de nitrato de prata 0,1mol/L.
Considere as seguintes substâncias:
I - água destilada;
II - solução de eosina;
III - solução de ácido acético;
IV - brometo de potássio.
É correto afirmar que o branco da titulação para essa análise deve conter:
Provas
Caderno Container